题目内容
某有机化合物的结构简式为: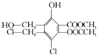 ,下列有关该物质的叙述正确的是( )
,下列有关该物质的叙述正确的是( )
 ,下列有关该物质的叙述正确的是( )
,下列有关该物质的叙述正确的是( )| A、1mol该物质最多可以消耗3 mol Na |
| B、1mol该物质最多可以消耗7 mol NaOH |
| C、不能与Na2CO3溶液反应 |
| D、易溶于水,可以发生加成反应和取代反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物含有醇羟基、酚羟基,可发生取代、氧化反应,含有酯基,可发生水解反应,含有-Cl,可发生取代反应,以此解答该题.
解答:
解:A.分子中含有2个羟基,可消耗2 mol Na,故A错误;
B.分子中含有1个酚羟基,2个酯基、1个-Cl,水解可生成2个酚羟基,2个羧基以及2个HCl,则1mol该物质最多可以消耗7 mol NaOH,故B正确;
C.含有酚羟基,可与Na2CO3溶液反应,故C错误;
D.含有酯基,不能溶于水,故D错误.
故选B.
B.分子中含有1个酚羟基,2个酯基、1个-Cl,水解可生成2个酚羟基,2个羧基以及2个HCl,则1mol该物质最多可以消耗7 mol NaOH,故B正确;
C.含有酚羟基,可与Na2CO3溶液反应,故C错误;
D.含有酯基,不能溶于水,故D错误.
故选B.
点评:本题考查有机物的结构和性质,为高频常见题型,侧重于学生的分析能力的考查,注意把握有机物官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下表中物质的分类组合完全正确的是( )
| 选项 | A | B | C | D |
| 强电解质 | KNO3 | H2SO4 | BaSO4 | HClO4 |
| 弱电解质 | HF | CaCO3 | HClO | CH3COONH4 |
| 非电解质 | SO2 | 金属Al | H2O | C2H5OH |
| A、A | B、B | C、C | D、D |
已知在一定条件下能发生下列反应:N2+3Mg
Mg3N2(固),空气缓缓通过下图装置时,依次除去的气体是( )
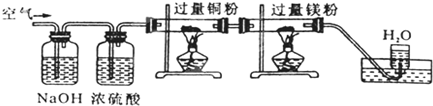
| ||

| A、CO2、H2O、O2、N2 |
| B、N2、O2、CO2、H2O |
| C、H2O、CO2、N2、O2 |
| D、CO2、N2、H2O、O2 |
Al粉投入某无色澄清的溶液中产生H2,则下列离子组合正确的是( )
| A、H+、Ca2+、Na+、CO32- |
| B、Na+、Mg2+、Al3+、Cl- |
| C、Cu2+、Mg2+、Cl-、OH- |
| D、Ba2+、Cl-、OH-、NO3- |
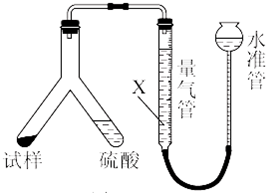
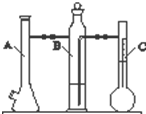 利用如图所示实验装置可以测定一定条件下1mol气体的体积.图中仪器C称为液体量瓶,瓶颈上有110~130mL刻度线.将一定质量的镁带和过量的稀硫酸在仪器A瓶中完全反应,产生的H2将B瓶中的液体压入液体量瓶中,根据液体的体积可以转换成H2的体积.
利用如图所示实验装置可以测定一定条件下1mol气体的体积.图中仪器C称为液体量瓶,瓶颈上有110~130mL刻度线.将一定质量的镁带和过量的稀硫酸在仪器A瓶中完全反应,产生的H2将B瓶中的液体压入液体量瓶中,根据液体的体积可以转换成H2的体积.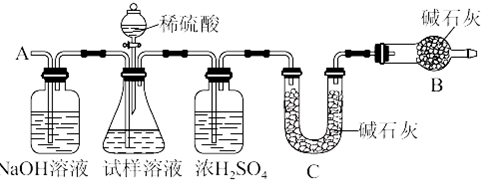
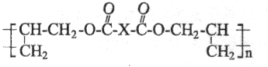

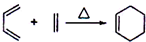 ; ii)CH2=CHCH3
; ii)CH2=CHCH3