题目内容
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A、氢氧化钠与盐酸;氢氧化铜与盐酸 |
| B、石灰石与硝酸反应;石灰石与盐酸反应 |
| C、BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 |
| D、Na2CO3溶液与硝酸溶液;CaCO3与硝酸溶液 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧化铜为沉淀,氢氧化钠易溶于水;
B.两个反应实质均为碳酸钙和氢离子反应;
C.氯化钡溶液与硫酸钠溶液反应生成硫酸钡和氯化钠,而氢氧化钡溶液与硫酸溶液反应生成硫酸钡和水;
D.碳酸钠为易溶性盐,碳酸钙难溶.
B.两个反应实质均为碳酸钙和氢离子反应;
C.氯化钡溶液与硫酸钠溶液反应生成硫酸钡和氯化钠,而氢氧化钡溶液与硫酸溶液反应生成硫酸钡和水;
D.碳酸钠为易溶性盐,碳酸钙难溶.
解答:
解:A.氢氧化铜为沉淀,应保留化学式;氢氧化钠易溶于水,应拆成离子形式,不能用同一离子反应表示,故A不选;
B.两个反应实质均为碳酸钙和氢离子反应,离子反应均为:CaCO3+2H+═H2O+CO2↑+Ca2+,故B选;
C.氯化钡溶液与硫酸钠溶液反应生成硫酸钡和氯化钠,而氢氧化钡溶液与硫酸溶液反应生成硫酸钡和水,水在离子反应中保留化学式,不能用同一离子反应表示,故C不选;
D.碳酸钠为易溶性盐,应拆成离子形式;碳酸钙难溶,应保留化学式,不能用同一离子反应表示,故D不选;
故选:B.
B.两个反应实质均为碳酸钙和氢离子反应,离子反应均为:CaCO3+2H+═H2O+CO2↑+Ca2+,故B选;
C.氯化钡溶液与硫酸钠溶液反应生成硫酸钡和氯化钠,而氢氧化钡溶液与硫酸溶液反应生成硫酸钡和水,水在离子反应中保留化学式,不能用同一离子反应表示,故C不选;
D.碳酸钠为易溶性盐,应拆成离子形式;碳酸钙难溶,应保留化学式,不能用同一离子反应表示,故D不选;
故选:B.
点评:本题考查离子反应方程式,明确发生的化学反应是解答本题的关键,注意掌握离子反应方程式的书写方法,难度不大.

练习册系列答案
相关题目
运用有关概念判断下列叙述正确的是( )
| A、1mol H2燃烧放出的热量为H2的燃烧热 |
| B、Na2SO3和H2O2的反应为氧化还原反应 |
C、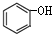 和 和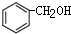 互为同系物 互为同系物 |
| D、BaSO4的水溶液不导电,故BaSO4是弱电解质 |
下列各组物质中,均为纯净物的一组是( )
| A、碘酒 干冰 |
| B、液氯 浓硫酸 |
| C、石灰石 氨水 |
| D、CuSO4?5H2O 冰水混合物 |
下列离子方程式正确的是( )
| A、Na2CO3 溶液中滴入少量盐酸:CO32-+H+═HCO3- |
| B、钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
| C、Ba(OH)2与稀H2SO4反应:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
| D、FeCl3溶液与Cu反应:Cu+Fe3+=Cu2++Fe2+ |
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、40g SO2气体所占的体积为11.2L |
| B、7.1gCl2与足量水反应转移电子数为0.1NA |
| C、1mol?L-1的CH3COONa溶液中,CH3COO-离子数小于NA |
| D、常温常压下,32gO2和O3的混合气体含氧原子数为2NA |
下列化学方程式书写正确,且反应类型正确的是( )
| A、Na2SO4+BaCl2═BaSO4↓+NaCl(复分解反应) | ||||
B、2KMnO4
| ||||
C、H2+CuO
| ||||
D、Mg+O2
|
下列关于摩尔质量的说法正确的是( )
| A、氯气的摩尔质量是71克 |
| B、氯化氢的摩尔质量为36.5 g/moL |
| C、1mol氢的质量为2克 |
| D、O2的摩尔质量为16g/moL |
用惰性电极实现电解,下列说法中正确的是( )
| A、电解硫酸铜溶液,加入CuO可使电解后的溶液恢复到原状态 |
| B、电解硝酸银溶液,在阴极上和阳极上析出产物的物质的量之比为1:2 |
| C、电解氯化钾溶液,要消耗H+,故溶液pH减小 |
| D、电解稀硫酸溶液,实质上是电解水,故溶液pH不变 |