题目内容
酸、碱、盐溶液能够导电,是因为物质溶于水时,离解成为自由移动的阴、阳离子.
(1)下列物质的电离方程式如下:
HClO4═H++ClO
; Ba(OH)2═Ba2++2OH-;
Fe2(SO4)3═2Fe3++3SO
; KHSO4═K++H++SO
.
属于酸的物质 (写化学式,下同);属于碱的物质为 ;属于盐的物质 .
(2)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱.
①从物质的分类角度看,不恰当的一种物质是 .
②上述物质中既不是电解质也不是非电解质的是 .依据是 .
③写出纯碱的电离方程式 .
(1)下列物质的电离方程式如下:
HClO4═H++ClO
- 4 |
Fe2(SO4)3═2Fe3++3SO
2- 4 |
2- 4 |
属于酸的物质
(2)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱.
①从物质的分类角度看,不恰当的一种物质是
②上述物质中既不是电解质也不是非电解质的是
③写出纯碱的电离方程式
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:(1)电离出来的阳离子全部是氢离子的化合物为酸,电离出的阴离子全部是氢氧根离子的化合物属于碱,盐是指由金属离子和酸根离子组成的化合物;
(2)①纯碱为Na2CO3,是由金属离子和酸根离子构成的;
②混合物既不是电解质,又不是非电解质;
③纯碱在溶液中完全电离出钠离子与碳酸根离子.
(2)①纯碱为Na2CO3,是由金属离子和酸根离子构成的;
②混合物既不是电解质,又不是非电解质;
③纯碱在溶液中完全电离出钠离子与碳酸根离子.
解答:
解:(1)电离出来的阳离子全部是氢离子的化合物为酸,则属于酸的物质为HClO4,电离出的阴离子全部是氢氧根离子的化合物属于碱,则属于碱的物质为Ba(OH)2,盐是指由金属离子和酸根离子组成的化合物,则属于盐的为 Fe2(SO4)3、KHSO4;
故答案为:HClO4;Ba(OH)2; Fe2(SO4)3、KHSO4;
(2)①纯碱为Na2CO3,是由金属离子和酸根离子构成的,属于盐,不是碱;故答案为:纯碱;
②混合物既不是电解质,又不是非电解质,盐酸是HCL的水溶液,既不是电解质也不是非电解质;
故答案为:盐酸;盐酸是混合物,不是化合物;
③纯碱在溶液中完全电离出钠离子与碳酸根离子,其电离方程式为:Na2CO3═2Na++CO32-;故答案为:Na2CO3═2Na++CO32-.
故答案为:HClO4;Ba(OH)2; Fe2(SO4)3、KHSO4;
(2)①纯碱为Na2CO3,是由金属离子和酸根离子构成的,属于盐,不是碱;故答案为:纯碱;
②混合物既不是电解质,又不是非电解质,盐酸是HCL的水溶液,既不是电解质也不是非电解质;
故答案为:盐酸;盐酸是混合物,不是化合物;
③纯碱在溶液中完全电离出钠离子与碳酸根离子,其电离方程式为:Na2CO3═2Na++CO32-;故答案为:Na2CO3═2Na++CO32-.
点评:本题考查物质的分类,熟悉根据物质的组成和性质得出的分类结果、物质的性质是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、氢键、分子间作用力、离子键、共价键都是微粒间的作用力.其中分子间作用力只影响物质的熔沸点而不影响物质的溶解性 |
| B、石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向 |
| C、结合质子能力由强到弱的顺序是OH->CH3COO->Cl- |
D、原子结构模型的演变经历了: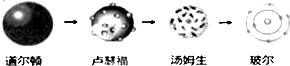 |
如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )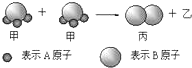

| A、根据阿伏加德罗定律可推知,1个乙分子中含有2个A原子 |
| B、该反应类型是分解反应 |
| C、该反应一定属于氧化还原反应 |
| D、Mr(甲)=Mr(乙)+Mr(丙) |
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A、氢氧化钠与盐酸;氢氧化铜与盐酸 |
| B、石灰石与硝酸反应;石灰石与盐酸反应 |
| C、BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 |
| D、Na2CO3溶液与硝酸溶液;CaCO3与硝酸溶液 |
下列说法正确的是( )
| A、Na和NaCl灼烧时,它们的焰色反应分别是黄色和无色 |
| B、在2Al+2H2O+2NaOH=2NaAlO2+3H2#中,氧化剂是H2O和NaOH |
| C、H2和Cl2只有在点燃条件下才可以反应 |
| D、在标准状况下,1 mol H2和O2混合气体,所占的体积约是22.4 L |
为迎接北京奥运,北京曾采用机动车按照单双号行驶的方案,该方案既保障了交通秩序,又大大减少了空气污染.汽车尾气中所含污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有( )
| A、氮气 | B、硫化氢 |
| C、二氧化硫 | D、氮的氧化物 |
 无机化合物可根据其组成和性质进行分类,以Na、H、O、N中任两种或三种元素组成合适的物质,分别填在下表②③的后面.
无机化合物可根据其组成和性质进行分类,以Na、H、O、N中任两种或三种元素组成合适的物质,分别填在下表②③的后面.