题目内容
某混合溶液中所含离子的浓度如表,则M离可能为( )
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度/(mol?L-1) | 2 | 1 | 2 | 1 |
| A、Cl- |
| B、Ba2+ |
| C、Na+ |
| D、Mg2+ |
考点:离子反应发生的条件,离子共存问题
专题:离子反应专题
分析:根据电解质混合溶液中阴阳离子所带电荷相等确定M离子所带电荷,并利用离子之间的反应来判断存在的离子.
解答:
解:溶液中,单位体积内已知的阳离子所带电量为:2mol/L×1=2mol/L,
单位体积内已知的阴离子所带总电量为:2mol/L×1+1mol/L×2=4mol/L,
阴离子所带电荷多,故M为阳离子,
设M离子的电荷为x,由电荷守恒可知:4=2+x×1,解得x=+2,
结合选项可知,M为Ba2+或Mg2+,又SO42-与Ba2+能结合生成硫酸钡沉淀,不能共存,则溶液中存在的离子为Mg2+,
故选D.
单位体积内已知的阴离子所带总电量为:2mol/L×1+1mol/L×2=4mol/L,
阴离子所带电荷多,故M为阳离子,
设M离子的电荷为x,由电荷守恒可知:4=2+x×1,解得x=+2,
结合选项可知,M为Ba2+或Mg2+,又SO42-与Ba2+能结合生成硫酸钡沉淀,不能共存,则溶液中存在的离子为Mg2+,
故选D.
点评:本题考查物质的量浓度的有关计算、离子共存,难度不大,利用电荷守恒确定M所带电荷是关键.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快是( )
| A、V(H2)═0.1mol/(L?min) |
| B、V(N2)═0.1mol/(L?min) |
| C、V(NH3)═0.15mol/(L?min) |
| D、V(N2)═0.002mol/(L?s) |
按下列实验方法能够达到要求的是( )
| A、用10mL量筒量取7.50mL稀盐酸 |
| B、用托盘天平称量出25.20g NaCl晶体 |
| C、用pH试纸测得某碱溶液的pH为12.7 |
| D、用25mL碱式滴定管量出14.08mL NaOH溶液 |
用银为电极电解盐酸时,下列说法正确的是( )
| A、溶液的pH升高 |
| B、同温、同压下两极上析出等体积的气体 |
| C、阴极质量增加 |
| D、溶液中c(Cl-)几乎不变 |
下列各物质能使酸性高锰酸钾溶液褪色,但不能使溴水因发生化学反应而褪色的是( )
| A、乙烷 | B、乙烯 | C、甲苯 | D、苯 |
已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-?H++B2-,下列说法正确的是( )
| A、Na2B溶液一定有:c(OH-)>c(H+)+c(HB-) |
| B、Na2B溶液一定呈碱性,NaHB溶液可能呈酸性也可能呈碱性 |
| C、NaHB溶液一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+c(B2-) |
| D、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性 |
下列图示中关于铜电极的连接错误的是( )
A、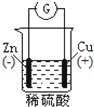 铜锌原电池 |
B、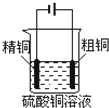 电解精炼铜 |
C、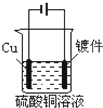 镀件上镀铜 |
D、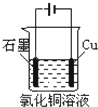 电解氯化铜溶液 |
 ⑤CH≡CH
⑤CH≡CH