题目内容
用银为电极电解盐酸时,下列说法正确的是( )
| A、溶液的pH升高 |
| B、同温、同压下两极上析出等体积的气体 |
| C、阴极质量增加 |
| D、溶液中c(Cl-)几乎不变 |
考点:电解原理
专题:电化学专题
分析:用Ag作电极电解稀盐酸时,阳极上银失电子发生氧化反应,电极反应式为Ag-e-+Cl-=AgCl↓,阴极上电极反应式为2H++2e-=H2↑,据此分析解答.
解答:
解:用Ag作电极电解稀盐酸时,阳极上银失电子发生氧化反应,电极反应式为Ag-e-+Cl-=AgCl↓,阴极上电极反应式为2H++2e-=H2↑,
A.阴极上电极反应式为2H++2e-=H2↑,导致溶液中氢离子浓度降低,则溶液的pH增大,故A正确;
B.负极上Ag放电没有气体生成,故B错误;
C.阴极上氢离子放电生成氢气,则阴极质量不变,故C错误;
D.阳极电极反应式为Ag-e-+Cl-=AgCl↓,则溶液中c(Cl-)减小,故D错误;
故选A.
A.阴极上电极反应式为2H++2e-=H2↑,导致溶液中氢离子浓度降低,则溶液的pH增大,故A正确;
B.负极上Ag放电没有气体生成,故B错误;
C.阴极上氢离子放电生成氢气,则阴极质量不变,故C错误;
D.阳极电极反应式为Ag-e-+Cl-=AgCl↓,则溶液中c(Cl-)减小,故D错误;
故选A.
点评:本题考查了电解原理,明确阴阳极上发生的电极反应式是解本题关键,再结合离子之间的反应分析解答,注意活泼金属作电极时阳极上发生的反应,为易错点.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、2.4g镁与足量的盐酸反应,电子转移数目为0.1NA |
| B、0.5mol/L的Na2SO4的溶液中含NA个Na+ |
| C、1molNa2O2固体中含2NA个阴离子 |
| D、1molCH5+离子所含电子数为10NA |
下列有关化学用语表示正确的是( )
A、3,3-二甲基-1-戊烯的键线式: |
B、甲醛的电子式: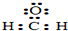 |
C、乙醇分子的比例模型: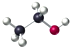 |
D、CH4Si的结构式: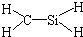 |
某混合溶液中所含离子的浓度如表,则M离可能为( )
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度/(mol?L-1) | 2 | 1 | 2 | 1 |
| A、Cl- |
| B、Ba2+ |
| C、Na+ |
| D、Mg2+ |
红热的碳与浓硫酸反应所产生的气体中可能含有CO、CO2、SO2、H2O等气体,用 ①无水CuSO4 ②澄清石灰水 ③红热CuO ④生石灰 ⑤品红溶液 ⑥酸性高锰酸钾溶液等药品可将其一一检出,检测时气体通入药品的正确顺序是( )
| A、①-⑤-②-⑥-⑤-④-③ |
| B、①-⑤-⑥-⑤-②-④-③ |
| C、③-④-②-⑤-⑥-⑤-① |
| D、②-⑤-①-④-③-⑥-⑤ |
饱和一元醇C7H15OH,发生消去反应时,若可以得到两种单烯烃,该醇的结构简式( )
A、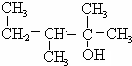 |
B、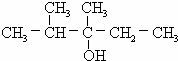 |
| C、CH3(CH2)5CH2OH |
D、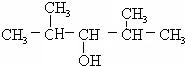 |
下列实验操作中,所用试剂正确的是( )
| A、用酒精萃取碘水中的碘 |
| B、用氯化钡溶液鉴别稀盐酸和稀硫酸 |
| C、用稀硫酸洗去残留在试管壁上的碳酸钙 |
| D、用稀盐酸鉴别碳酸钠溶液和碳酸钾溶液 |
鉴别NO2气体和Br2蒸气,可用 ( )
①湿润的淀粉KI试纸 ②AgNO3溶液 ③水 ④烧碱溶液.
①湿润的淀粉KI试纸 ②AgNO3溶液 ③水 ④烧碱溶液.
| A、①④ | B、③④ | C、②③ | D、全部 |