题目内容
向体积为Va的0.05mol?L-1CH3COOH溶液中加入体积为Vb的0.05mol?L-1KOH溶液,下列关系正确的是( )
| A、Va=Vb时:c (CH3COO-)=c (K+) |
| B、Va=Vb时:c (CH3COOH)+c (H+)=c (OH-) |
| C、Va>Vb时:c (CH3COO-)>c (K+)>c (OH-)>c (H+) |
| D、Va与Vb任意比时:c (K+)+c (H+)=c (OH-)+c (CH3COO-) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.当Va=Vb时,酸和碱恰好中和,溶液中的溶质是醋酸钾,根据醋酸钾溶液中各离子浓度进行判断;
B.当Va=Vb时,酸和碱恰好中和,溶液中的溶质是醋酸钾,根据质子守恒判断正误;
C.酸和碱的物质的量浓度相等,且都是一元的,当Va>Vb时,酸过量,溶液中的溶质是醋酸钾和醋酸,根据电荷守恒判断溶液中离子浓度大小;
D.Va和Vb为任意比时,根据电荷守恒判断正误.
B.当Va=Vb时,酸和碱恰好中和,溶液中的溶质是醋酸钾,根据质子守恒判断正误;
C.酸和碱的物质的量浓度相等,且都是一元的,当Va>Vb时,酸过量,溶液中的溶质是醋酸钾和醋酸,根据电荷守恒判断溶液中离子浓度大小;
D.Va和Vb为任意比时,根据电荷守恒判断正误.
解答:
解:A.当Va=Vb时,酸和碱恰好中和,溶液中的溶质是醋酸钾,由于醋酸根离子部分水解,导致醋酸根离子浓度减小,则c (CH3COO-)<c (K+),故A错误;
B.根据醋酸钾溶液中的质子守恒知:c(CH3COOH)+c(H+)=c(OH-),故B正确;
C.Va>Vb时,如果c(CH3COO-)>c(K+)>c(OH-)>c(H+),不满足电荷守恒,即:如果c(CH3COO-)>c(K+),则c(OH-)<c(H+),故C错误;
D.Va和Vb为任意比时,溶液呈电中性,溶液中阴阳离子所带电荷相等,根据电荷守恒得:c(K+)+c(H+)=c(OH-)+c(CH3COO-),故D正确;
故选BD.
B.根据醋酸钾溶液中的质子守恒知:c(CH3COOH)+c(H+)=c(OH-),故B正确;
C.Va>Vb时,如果c(CH3COO-)>c(K+)>c(OH-)>c(H+),不满足电荷守恒,即:如果c(CH3COO-)>c(K+),则c(OH-)<c(H+),故C错误;
D.Va和Vb为任意比时,溶液呈电中性,溶液中阴阳离子所带电荷相等,根据电荷守恒得:c(K+)+c(H+)=c(OH-)+c(CH3COO-),故D正确;
故选BD.
点评:本题考查了混合溶液中离子浓度大小的比较,属于中等难度,要求学生能够根据盐的水解原理、物料守恒、电荷守恒、质子守恒等比较溶液中给离子浓度大小.

练习册系列答案
相关题目
能正确表示下列化学反应的离子方程式是( )
| A、饱和石灰水跟稀硝酸反应 Ca(OH)2+2H+═Ca2++2H2O |
| B、钠和水反应 Na+2H2O═Na++H2↑+2OH- |
| C、大理石与盐酸反应CaCO3+2H+═Ca2++H2O+CO2↑ |
| D、硫酸与氢氧化钡溶液反应Ba2++OH-+H++SO42-═BaSO4↓+H2O |
下列说法正确的是( )
| A、铜锌原电池工作时,若有6.5g锌被溶解,电路中就有0.1mol电子通过 |
| B、55号元素位于周期表的第六周期第IIA族 |
| C、可利用CH4和O2的反应设计成原电池 |
| D、在周期表中金属和非金属的分界处易寻找到催化剂和耐高温、耐腐蚀的合金材料 |
下列实验操作或装置错误的是( )
A、 蒸馏 |
B、 过滤 |
C、 萃取 |
D、 转移溶液 |
相同物质的量的钠、镁、铝与过量的稀硫酸反应,在标况下产生氢气的体积比是( )
| A、1:1:1 |
| B、1:2:3 |
| C、6:3:2 |
| D、23:24:27 |
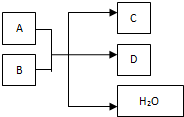 在一定条件下,某些化学反应可用如图表示,请回答下列问题
在一定条件下,某些化学反应可用如图表示,请回答下列问题