题目内容
相同物质的量的钠、镁、铝与过量的稀硫酸反应,在标况下产生氢气的体积比是( )
| A、1:1:1 |
| B、1:2:3 |
| C、6:3:2 |
| D、23:24:27 |
考点:化学方程式的有关计算,常见金属元素的单质及其化合物的综合应用
专题:几种重要的金属及其化合物
分析:相同物质的量的钠、镁、铝分别与足量的稀硫酸反应,依据电子守恒计算生成氢气气体体积比.
解答:
解:相同物质的量的钠、镁、铝分别与足量的稀硫酸反应,
Na~Na+~e-~0.5H2
Mg~Mg2+~2e-~H2
Al~Al3+~3e-~1.5H2
所以相同物质的量的钠、镁、铝分别与足量的稀硫酸反应生成相同状况下氢气的体积比=物质的量之比=0.5:1:1.5=1:2:3,
故选B.
Na~Na+~e-~0.5H2
Mg~Mg2+~2e-~H2
Al~Al3+~3e-~1.5H2
所以相同物质的量的钠、镁、铝分别与足量的稀硫酸反应生成相同状况下氢气的体积比=物质的量之比=0.5:1:1.5=1:2:3,
故选B.
点评:本题考查了金属和酸反应的定量关系分析计算应用,应用电子守恒直接就是定量关系是较简洁的方法,题目较简单.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、Cu(OH)2中加入硫酸:OH-+H+═H2O |
| B、钠加入水中:Na+2H2O═Na++2OH-+H2↑ |
| C、FeSO4溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
| D、Al2(SO4)3溶液中加入足量Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
已知:25℃时,Ka(HAc)=1.7×10-5 mol?L-1.现有如下溶液:
①0.1mol?L-1 HAc与0.1mol?L-1NaOH溶液等体积混合液
②pH=3的HAc与pH=11的NaOH溶液等体积混合液
③0.1mol?L-1 H2SO4与0.2mol?L-1 NaOH溶液等体积混合液
常温时,三者pH大小关系正确的是( )
①0.1mol?L-1 HAc与0.1mol?L-1NaOH溶液等体积混合液
②pH=3的HAc与pH=11的NaOH溶液等体积混合液
③0.1mol?L-1 H2SO4与0.2mol?L-1 NaOH溶液等体积混合液
常温时,三者pH大小关系正确的是( )
| A、①>③>② |
| B、③>①>② |
| C、①>②>③ |
| D、②>③>① |
下列离子方程式书写正确的是( )
| A、Cl2通入Na2SO3溶液:2Cl2+H2O+SO32-═2HClO+SO2↑+2Cl- |
| B、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
C、水杨酸(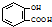 )中加入Na2CO3溶液: )中加入Na2CO3溶液: +CO32-→ +CO32-→ +CO2↑+H2O +CO2↑+H2O |
| D、SO2通入酸性高锰酸钾溶液:5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+ |
向体积为Va的0.05mol?L-1CH3COOH溶液中加入体积为Vb的0.05mol?L-1KOH溶液,下列关系正确的是( )
| A、Va=Vb时:c (CH3COO-)=c (K+) |
| B、Va=Vb时:c (CH3COOH)+c (H+)=c (OH-) |
| C、Va>Vb时:c (CH3COO-)>c (K+)>c (OH-)>c (H+) |
| D、Va与Vb任意比时:c (K+)+c (H+)=c (OH-)+c (CH3COO-) |
 氮气及含氮的化合物在国民经济中占有重要地位.合成氨工业中,合成塔中每产生2mol NH3,放出92.4kJ热量.
氮气及含氮的化合物在国民经济中占有重要地位.合成氨工业中,合成塔中每产生2mol NH3,放出92.4kJ热量. 丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活.
丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活.