题目内容
1.请回答下列问题:(1)写出NH4Cl的电子式
 ;
;(2)用电子式表示H2O的形成过程
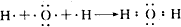 ;
;(3)已知一定条件下,白磷转化为红磷释放出能量,则等质量的白磷比红磷具有的能量高(填“高”、“低”),故白磷比红磷稳定性弱(填“强”、“弱”),等质量的白磷和红磷充分燃烧均生成五氧化二磷,白磷放出热量多.
分析 (1)氯化铵为离子晶体,由氨根离子与氯离子通过离子键结合在一起;
(2)水是共价化合物,H与O原子之间形成一对共用电子对,据此写出用电子式表示H2O的形成过程;
(3)放热反应中,反应物总能量大于生成物总能量,则白磷能量高;物质的能量越高,该物质越不稳定;生成物相同时,反应物总能量越高,则反应中放热热量越高.
解答 解:(1)氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ,
,
故答案为: ;
;
(2)H2O为共价化合物,各原子达到稳定结构,其分子中存在两个氧氢键,用电子式表示形成过程为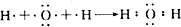 ,
,
故答案为: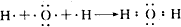 ;
;
(3)已知一定条件下,白磷转化为红磷释放出能量,说明反应物能量大于生成物总能量,则等质量的白磷比红磷具有的能量高,能量越高的物质越不稳定,故白磷比红磷稳定性弱;等质量的白磷和红磷充分燃烧均生成五氧化二磷,由于白磷能量高,属于白磷放出热量多,
故答案为:高、弱、白磷.
点评 本题考查了电子式的表示方法及其应用、化学反应与能量变化等知识,题目难度中等,注意掌握电子式的能够及书写原则,明确化学反应与能量变化的关系及物质稳定性与能量大小的关系.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
12.下列说法正确的是( )
| A. | 氯化钾溶液在电流作用下电离成钾离子和氯离子 | |
| B. | 二氧化硫溶于水能部分转化成离子,故二氧化硫属于弱电解质 | |
| C. | 纯净的电解质在液态时,有的导电有的不导电 | |
| D. | 硫酸钡难溶于水,所以硫酸钡属弱电解质 |
6.下列各组微粒中,电子总数相同的是( )
| A. | F-、Cl-、Br-、I- | B. | S2-、Ca2+、Ar、Cl- | ||
| C. | Na+、K+、Mg2+、Al3+ | D. | Mg2+、Mg、Al3+、Al |
13.图是某只含有C、H、O元素的有机物简易球棍模型,下列关于该有机物的说法正确的是( )
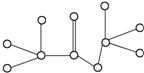

| A. | 分子式为C3H8O2 | |
| B. | 该物质属于酯类 | |
| C. | 该物质可由乙酸与乙醇反应制得 | |
| D. | 该物质含有双键,能跟氢气发生加成反应 |
10.对于反应:2H2S+SO2═3S+2H2O,被氧化的硫原子与被还原的硫原子的质量之比为( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 1:2 |
 .
.