��Ŀ����
���мס�������ʵ�飬���з�ӦN2(g)+3H2(g)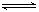 2NH3(g)������������ʵ�飬���з�ӦH2(g)+I2(g)
2NH3(g)������������ʵ�飬���з�ӦH2(g)+I2(g) 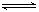 2HI(g) ?H=-akJ?mol��1,ʵ����������ʼͶ�����±���ʾ�����½�����ȷ����
2HI(g) ?H=-akJ?mol��1,ʵ����������ʼͶ�����±���ʾ�����½�����ȷ����

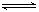 2NH3(g)������������ʵ�飬���з�ӦH2(g)+I2(g)
2NH3(g)������������ʵ�飬���з�ӦH2(g)+I2(g) 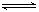 2HI(g) ?H=-akJ?mol��1,ʵ����������ʼͶ�����±���ʾ�����½�����ȷ����
2HI(g) ?H=-akJ?mol��1,ʵ����������ʼͶ�����±���ʾ�����½�����ȷ����
| A�������У���ƽ��ʱN2��NN3��ת���ʷֱ�Ϊ��1 �ͦ�2�����1 +��2=1 |
| B�������У�ƽ�����NH3��Ũ����ƽ���Ķ��� |
| C�������У�����ƽ��ʱ���з���Q1kJ, ��������Q2kJ����Q1+Q2=a |
| D�������У���ƽ������ʱ�䣺��С�ڢ� |
C
���DZ��ֺ��º��ݵģ���Ϊ4mol�����൱����2mol������6mol���������Լ���I����ƽ���Dz���Ч�ģ����1 +��2������1��A����ȷ�������У�ѹǿ���¶Ȳ��䣬����ƽ���ǵ�Ч�ģ�����ƽ�����NH3��Ũ�Ⱥ�ƽ�����NH3��Ũ����ȣ�B����ȷ������2molHI�൱����1mol������1mol�⣬���ƽ���ǵ�Ч�ģ�����C��ȷ�������У�ѹǿ���¶Ȳ��䣬����������ݻ��DZ仯�ģ���Ӧ���Ũ������ͬ�ģ���ƽ������ʱ����ͬ��������ȷ�Ĵ�ѡC��

��ϰ��ϵ�д�
�����Ŀ
 2 Z����ƽ�ⳣ��Ϊ1600
2 Z����ƽ�ⳣ��Ϊ1600 C��g��+D��g�����ڲ�ͬ�¶��£�D�����ʵ���n��D����ʱ��t�Ĺ�ϵ��ͼ���Իش��������⣺
C��g��+D��g�����ڲ�ͬ�¶��£�D�����ʵ���n��D����ʱ��t�Ĺ�ϵ��ͼ���Իش��������⣺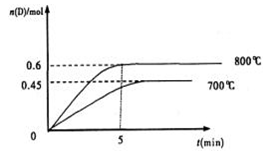
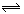 N2O4(g) ��H��0 ����ƿ����100���ˮ�У��ֽ����µ�ƽ��״̬��ǰ����ƽ��Ƚϣ�������ǣ� ��
N2O4(g) ��H��0 ����ƿ����100���ˮ�У��ֽ����µ�ƽ��״̬��ǰ����ƽ��Ƚϣ�������ǣ� �� 2SO3(g) ��H<0����֪c(SO2)ʼ=0.4mol/L��c(O2)ʼ=1mol/L���ⶨ�÷�Ӧ�ڸ��¶��µ�ƽ�ⳣ��K��19�����жϣ�
2SO3(g) ��H<0����֪c(SO2)ʼ=0.4mol/L��c(O2)ʼ=1mol/L���ⶨ�÷�Ӧ�ڸ��¶��µ�ƽ�ⳣ��K��19�����жϣ� C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£� 2C(g) ��H��0��
2C(g) ��H��0��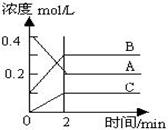
 CO2��H2.����Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����
CO2��H2.����Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����