题目内容
14.将BaO2放入密闭真空容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )| A. | 平衡常数减小 | B. | BaO2量不变 | C. | 氧气压强不变 | D. | BaO量不变 |
分析 保持温度不变,缩小容器体积,增大压强,可逆反应向逆反应方向移动,化学平衡常数只与温度有关,据此分析解答.
解答 解:A.化学平衡常数只与温度有关,温度不变,平衡常数不变,故A错误;
B.缩小容器体积,增大压强,平衡向逆反应方向移动,则BaO的量减小,故B错误;
C.平衡向逆反应方向移动,但温度不变,平衡常数不变,氧气浓度不变,其压强不变,故C正确;
D.平衡向逆反应方向移动,则BaO2量增加,故D错误;
故选C.
点评 本题考查了可逆反应平衡移动,根据压强与平衡移动方向之间的关系分析解答即可,注意平衡常数只与温度有关,与物质浓度无关,为易错点,题目难度中等.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
5.反应4NH3+5O2?4NO+6H2O在一定体积的密闭容器中进行,30s后NO的物质的量浓度增加了3mol/L,则下列反应速率正确的是( )
| A. | v (O2)=0.0125 mol•(L•s)-1 | B. | v (NO)=0.01mol•(L•s)-1 | ||
| C. | v (H2O)=0.12 mol•(L•s)-1 | D. | v(NH3)=0.1 mol•(L•s)-1 |
6.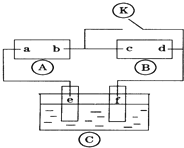 图中
图中 为直流电,
为直流电, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀池.接通电路后发现
为电镀池.接通电路后发现 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是( )
后,使c、d两点短路.下列叙述正确的是( )
 图中
图中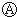 为直流电,
为直流电,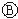 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀池.接通电路后发现
为电镀池.接通电路后发现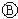 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是( )
后,使c、d两点短路.下列叙述正确的是( )| A. | b为直流电的正极 | B. | e电极为铁 | ||
| C. | f极发生还原反应 | D. | d极发生的反应为:2H++2e-=H2↑ |
1.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在1 mol CaC2、KHSO4的混合物中含阴、阳离子的总数为3NA | |
| B. | 0.1 mol C2H5OH中所含C-H键的数目为0.6NA | |
| C. | S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA | |
| D. | 78gNa2O2与足量水反应转移的电子数为2NA |
1.下列离子方程式中,正确的是( )
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 三氯化铁溶液中加入铁粉:Fe3++Fe═2 Fe2+ | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
 Ⅰ、某化学实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和反应反应热的测定
Ⅰ、某化学实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和反应反应热的测定
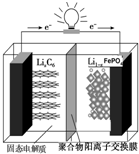 磷酸铁锂动力电池(LiFePO4电池)的内部结构如图所示.中间是聚合物的隔膜,它把正极与负极隔开,锂离子可以通过而电子不能通过.该电池的总反应式为:Li1-xFePO4+LixC6═C6+LiFePO4
磷酸铁锂动力电池(LiFePO4电池)的内部结构如图所示.中间是聚合物的隔膜,它把正极与负极隔开,锂离子可以通过而电子不能通过.该电池的总反应式为:Li1-xFePO4+LixC6═C6+LiFePO4