题目内容
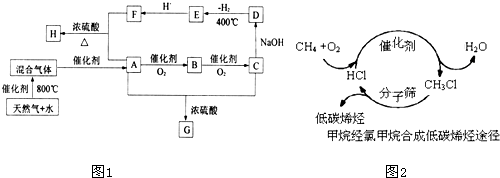
某混合物M,含有MgCl2、Al2O3,和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:

(1)试写出沉淀A、B、C的化学式:A 、B 、C .
(2)写出溶液→C反应的离子方程式: .

(1)试写出沉淀A、B、C的化学式:A
(2)写出溶液→C反应的离子方程式:
考点:几组未知物的检验
专题:元素及其化合物
分析:MgCl2、Al2O3,和Fe2O3中,Al2O3和Fe2O3不溶于水,氯化镁溶于水,可以和氢氧化钠反应生成氢氧化镁沉淀,即C是氢氧化镁,氧化铝可以和氢氧化钠反应得到偏铝酸钠,氧化铁不溶于氢氧化钠,所以A是氧化铁,向偏铝酸钠中加少量的盐酸可以得到氢氧化铝沉淀,即B是氢氧化铝,据此回答判断.
解答:
解:MgCl2、Al2O3,和Fe2O3中,Al2O3和Fe2O3不溶于水,氯化镁溶于水,可以和氢氧化钠反应生成氢氧化镁沉淀,即C是氢氧化镁,氧化铝可以和氢氧化钠反应得到偏铝酸钠,氧化铁不溶于氢氧化钠,所以A是氧化铁,向偏铝酸钠中加少量的盐酸可以得到氢氧化铝沉淀,即B是氢氧化铝,
(1)沉淀A、B、C分别是:氧化铁、氢氧化铝、氢氧化镁,故答案为:Fe2O3;Al(OH)3;Mg(OH)2.
(2)氯化镁可以和氢氧化钠反应生成氢氧化镁沉淀,即Mg2++2OH-=Mg(OH)2↓,故答案为:Mg2++2OH-=Mg(OH)2↓.
(1)沉淀A、B、C分别是:氧化铁、氢氧化铝、氢氧化镁,故答案为:Fe2O3;Al(OH)3;Mg(OH)2.
(2)氯化镁可以和氢氧化钠反应生成氢氧化镁沉淀,即Mg2++2OH-=Mg(OH)2↓,故答案为:Mg2++2OH-=Mg(OH)2↓.
点评:本题是一道物质的鉴别题目,注意物质的性质以及反应的现象是解题的关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
当今世界,环境问题日趋严峻,发展“低碳”经济,实现可持续发展已成为人们的共识.下列施可以提高燃料燃烧效率的是①通入适量的空气②提高燃料的着火点③降低燃料的着火点④将煤气化处理⑤将液体燃料化⑥将固体燃料粉碎( )
| A、①④⑤⑥ | B、①②③④ |
| C、③④⑤⑥ | D、②④⑤⑥ |
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700°C时反应制造出纳米级金刚石粉末和另一种化合物.该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻草变黄金”.同学们对此有以下“理解”,你认为其中错误的是( )
| A、该反应可能在空气中进行 |
| B、制造过程中元素种类没有改变 |
| C、另一种化合物是NaCl |
| D、这个反应是置换反应 |