题目内容
4.下列有关溶液中离子存在和转化的表达合理的是( )| A. | 中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- | |
| B. | 离子方程式2Ca2++3HCO3-+3OH-═2CaCO3↓+CO32-+3H2O可以表示NH4HCO3与澄清石灰水反应 | |
| C. | 由水电离出的c(H+)=1×10-12mol/L的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| D. | n[NH4AlSO4)2]:n[Ba(OH)2]=2:5 时发生的反应为NH4+Al3++2SO42-+2Ba2++5OH-═NH3•H2O+AlO2-+2H2O+BaSO4↓ |
分析 A.铁离子只能存在于酸性溶液中;
B.铵根离子也能够与氢氧根离子反应;
C.该溶液中存在大量氢离子或氢氧根离子,镁离子与氢氧根离子反应,酸性条件下硝酸根离子能够氧化碘离子;
D.n[NH4AlSO4)2]:n[Ba(OH)2]=2:5时,氢氧化钡过量,离子方程式按照NH4AlSO4)2的组成书写.
解答 解:A.Fe3+发生水解,只能存在酸性溶液中,故A错误;
B.若氢氧化钙不足时发生反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O,若氢氧化钙过量时发生反应:NH4++Ca2++HCO3-+2OH-═CaCO3↓+NH3•H2O+H2O↓,则题中说法错误,故B错误;
C.由水电离出的c(H+)=1×10-12mol/L的溶液呈酸性或碱性,Mg2+与氢氧根离子反应,酸性条件下I-、NO3-发生氧化还原反应,在溶液中一定不能大量共存,故C错误;
D.n[NH4AlSO4)2]:n[Ba(OH)2]=2:5 时,氢氧化钡完全过量,反应生成一水合氨按、偏铝酸钡、硫酸钡沉淀和水,发生的反应为:NH4++Al3++2SO42-+2Ba2++5OH-═NH3•H2O+AlO2-+2H2O+BaSO4↓,故D正确;
故选D.
点评 本题考查离子共存的正误判断、离子方程式的书写,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,掌握离子方程式的书写原则,试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
3.下列实验说法正确的是( )
| A. | 向2mL10%的NaOH溶液中滴加2%CuSO4溶液4~6滴制得新制氢氧化铜悬浊液 | |
| B. | 将Al2(SO4)3溶液蒸干、灼烧至恒重,最终剩余固体是Al2O3 | |
| C. | 将水蒸气通过灼热的铁粉,铁粉变红棕色,说明铁与水在高温下能发生反应 | |
| D. | 取a克Na2CO3和NaHCO3混合物与少量稀盐酸充分反应,加热、蒸干、灼烧至熔化,冷却得b克固体,可测得Na2CO3质量分数 |
12. 常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )
常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )
 常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )
常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )| A. | MOH为一元强碱 | |
| B. | N点水的电离程度大于K点水的电离程度 | |
| C. | 该温度下HA的电离平衡常数为5×10-6mo1•L-1 | |
| D. | 若K点对应溶液的pOH=10,则有c(HA)+c(H+)-c(OH-)=0.01mol•L-1 |
19.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 在电解精炼铜时,当电路中通过的电子数为2NA时,阳极质量减少64g | |
| B. | 标准状况下,22.4 LCO和C2H4混合气体的总分子数为NA,质量为28g | |
| C. | 常温常压下,1mol甲基(-CH3)所含电子数为10NA | |
| D. | 标准状况下,11.2L苯中含有C-H键的数目为3NA |
9.下列关于石灰石和熟石灰用途的说法中,错误的是( )
| A. | 燃煤时加入石灰石,可减少硫氧化物的排放 | |
| B. | 氯水中加入适量石灰石,可增强氯水的漂白性 | |
| C. | 酸性土壤中加入适量的熟石灰,可以中和其酸性 | |
| D. | 盐碱地(含较多NaCl、Na2CO3)中施用熟石灰,可降低土壤的碱性 |
16.某有机物结构简式如图,下列关于该有机物的说法正确的是( )


| A. | 苯环上的一溴代物有6种 | B. | 该分子中的所有碳原子可能共平面 | ||
| C. | 该有机物的分子式为C16H17O5 | D. | l mol该有机物可消耗3molNaOH |
13.今年4月22日是第48个世界地球日,我国确定的活动主题为“节约集约利用资源,倡导绿色简约生活--讲好我们的地球故事”.下列行为不符合这一活动主题的是( )
| A. | 推广使用清洁能源 | B. | 大力发展燃煤发电 | ||
| C. | 循环高效利用费源 | D. | 倡导环保低碳生活 |
14.已知反应2X(g)+Y(g)?2Z(g)△H的能量变化如图所示,下列分析正确的是( )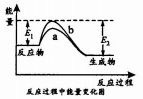

| A. | △H=+|E1-E2| | |
| B. | 曲线a为催化剂时的反应 | |
| C. | X(g)的能量高于Z(g)的能量 | |
| D. | 反应物吸收的总能量大于生成物释放的总能量 |
 $→_{②}^{NaOH,乙醇,△}$
$→_{②}^{NaOH,乙醇,△}$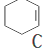 $→_{③}^{溴CCl_{4}溶液}$D$\stackrel{④}{→}$
$→_{③}^{溴CCl_{4}溶液}$D$\stackrel{④}{→}$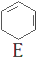
 ,名称是环己烷;
,名称是环己烷; ;B水解的化学方程式为
;B水解的化学方程式为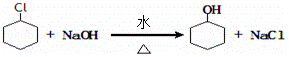 .
.