题目内容
6.氧化还原反应的实质是( )| A. | 氧原子的得失 | B. | 化合价的升降 | ||
| C. | 分子中原子重新组合 | D. | 电子的转移 |
分析 氧化还原反应的特征为化合价的升降,其实质为电子的转移,以此来解答.
解答 解:化合价的升降为氧化还原反应的特征,在氧化还原反应,形成共用电子对时发生电子的偏移,形成离子键时往往发生电子的得失,统称为电子的转移,为氧化还原反应的实质.
故选D.
点评 本题考查氧化还原反应的实质,明确实质为电子的转移,特征为化合价的升降即可解答,题目较简单.

练习册系列答案
相关题目
4.将下列每组内的四种物质同时加入到水中,充分搅拌后,既有氧化还原反应发生,又有沉淀产生的一组是( )
| A. | Na2O2、NH4Cl、NaCl、Na2SO4 | B. | FeO、AlCl3、Na2SiO3、硝酸 | ||
| C. | KHCO3、Ca(OH)2、MgCl2、硫酸 | D. | NaCO3、BaCl2、K2S、盐酸 |
14.下列各组离子在指定的溶液中一定能大量共存的是( )
| A. | 与铝粉反应放出氢气的无色溶液中:NO3-、Al3+、Na+、SO42- | |
| B. | 使红色石蕊试纸变蓝的溶液SO42-、HCO3-、Na+、K+ | |
| C. | 中性溶液:Fe3+、Al3+、NO3-、SO42- | |
| D. | 常温下,$\frac{C({H}^{+})}{C(O{H}^{-})}$=10-12的溶液:K+、AlO2-、CO32-、Na+ |
11.下列反应中氯气既作氧化剂又作还原剂的是( )
| A. | 用氯气制备漂白粉 | B. | 氯气和铜 | ||
| C. | 氯气和氢气 | D. | 浓盐酸与二氧化锰反应生成氯气 |
18.下列有关化学用语能确定为丙烯的是( )
| A. | 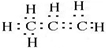 | B. | C3H6 | C. |  | D. |  |
15.如图是NaCl、NH4Cl和NaHCO3的溶解度曲线,下列说法不正确的是( )
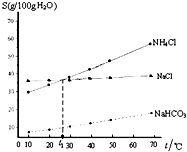

| A. | t1℃时,饱和NaCl和NH4Cl 溶液的物质的量浓度相同 | |
| B. | 相同温度下,NaHCO3在水中的溶解度比NaCl和NH4Cl小很多 | |
| C. | NH4Cl 溶解度随温度变化较大 | |
| D. | 工业上制纯碱可以向饱和的NaCl溶液中通入NH3和CO2,会有NaHCO3固体析出 |
16.中学化学中很多“规律”都有其使用范围,据有关“规律”下列结论合理的是( )
| A. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO | |
| B. | 金属钠可以通过电解熔融NaCl制得,推出金属铝可以通过电解熔融AlCl3制得 | |
| C. | 金属钠在纯氧中燃烧生成Na2O2,推出金属锂在纯氧中燃烧生成Li2O2 | |
| D. | CaCO3与稀硝酸反应生成CO2,推出CaSO3也能与稀硝酸反应生成SO2 |


