题目内容
2013年2月朝鲜进行了第三次核试验,引起国际社会的极大关注.235 92U是一种重要的核燃料,
U和
U的关系是( )
235 92 |
238 92 |
| A、中子数相同 |
| B、同种原子 |
| C、同位素 |
| D、同种核素 高温 |
考点:同位素及其应用
专题:原子组成与结构专题
分析:有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;
核素是指具有一定数目质子和一定数目中子的一种原子.
核素是指具有一定数目质子和一定数目中子的一种原子.
解答:
解:A.
U质子数为92,中子数为235-92=143,
U质子数为92,中子数为235-92=146,故中子数不同,故A错误;
B.
U和
U质子数相同,中子数不同,故是两种不同的原子,故B错误;
C.
U和
U质子数相同,中子数不同,故互为同位素,故C正确;
D.
U和
U是两种不同的原子,即两种核素,故D错误,
故选C.
235 92 |
238 92 |
B.
235 92 |
238 92 |
C.
235 92 |
238 92 |
D.
235 92 |
238 92 |
故选C.
点评:本题考查同位素、核素的概念,难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
气体A、B分别为0.6mol和0.5mol,在0.4L密闭容器中发生反应:3A+B?aC+2D,经5min后,此时气体C为0.2mol;又知在此反应时间内,D的平均反应速率为0.1mol/(L?min),下面的结论正确的是( )
| A、此时,反应混合物总物质的量为1mol |
| B、B反应的物质的量为0.1mol |
| C、A的平均反应速率为0.1mol/(L?min) |
| D、a值为1 |
下列实验操作中,错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出后,换个洁净的烧杯,将上层液体从上口放入烧杯中 |
| B、蒸馏时,应使温度计水银球位于蒸馏烧瓶支管口处 |
| C、用酒精萃取溴水溶液中的溴 |
| D、称量时,将称量物体放在称量纸或烧杯中,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
已知还原性S2->I->Fe2+>Br->Cl-,下列判断不正确的是( )
| A、Fe3+与I-在水溶液中不能大量共存 |
| B、氧化性:Cl2>Br2>I2 |
| C、将足量Br2加入到FeCl2溶液中,离子反应方程式为Br2+2Cl-═2Br-+Cl2 |
| D、将Cl2通入到FeBr2溶液中,Cl2应优先氧化Fe2+,再氧化Br- |
下列实验装置或操作能达到实验目的是( )
A、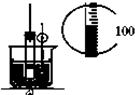 实验室制硝基苯 |
B、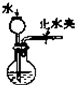 检查装置气密性 |
C、 利用排空气法收集丙烷 |
D、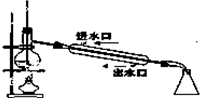 石油分馏 |
下列离子方程式中,正确的是( )
| A、铁跟稀H2SO4反应:2Fe+6H+=2Fe3++3H2↑ |
| B、碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、铜与硝酸银溶液反应:Cu+Ag+=Cu2++Ag |
| D、氢氧化钡溶液与稀H2SO4 反应:Ba2++SO42-=BaSO4↓ |
下列各组离子中,因发生氧化还原反应而不能大量共存的是( )
| A、K+、H+、I-、MnO4- |
| B、Fe3+、Fe2+、SO42-、NO3- |
| C、Al3+、Na+、SO42-、CO32- |
| D、Fe3+、H+、SO42-、ClO- |
已知:
①2H2(g)+O2(g)→2H2O(g)+483.6kJ;
②H2(g)+S(g)→H2S(g)+20.1kJ.
下列判断一定正确的是( )
①2H2(g)+O2(g)→2H2O(g)+483.6kJ;
②H2(g)+S(g)→H2S(g)+20.1kJ.
下列判断一定正确的是( )
| A、1mol氢气完全燃烧吸热246.8 kJ |
| B、1mol水蒸气和1mol硫化氢的能量相差221.7 kJ |
| C、由①②知,水的热稳定性小于硫化氢 |
| D、若反应②中改用固态硫,放热将小于20.1 kJ |