题目内容
13.以下对电子转移的方向和数目的表示正确的是( )| A. |  | B. |  | ||
| C. | 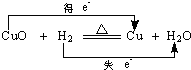 | D. |  |
分析 A.反应中Cl元素化合价由+5价变化为-1价,O元素化合价由-2价升高为0价;
B.Zn失去电子,H得到电子;
C.Cu元素化合价由+2价降低为0价,得到2个电子;
D.Cl元素的化合价由+5降低为0,得到电子,HCl中Cl失去电子.
解答 解:A.反应中Cl元素化合价由+5价变化为-1价,O元素化合价由-2价升高为0价,转移电子数目为12,故A正确;
B.Zn失去电子,H得到电子,转移电子数目为2,故B错误;
C.Cu元素化合价由+2价降低为0价,得到2个电子,氢气失去2个电子,故C错误;
D.Cl元素的化合价由+5降低为0,得到电子,HCl中Cl失去电子,转移电子数目为5,故D错误.
故选A.
点评 本题考查氧化还原反应转移电子数,为高频考点,侧重于学生的分析能力的考查,明确得失电子及数目为解答的关键,注意把握双线桥法标电子转移方法、数目的方法,题目难度不大.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
1.观察下列几个装置示意图,有关叙述正确的是( )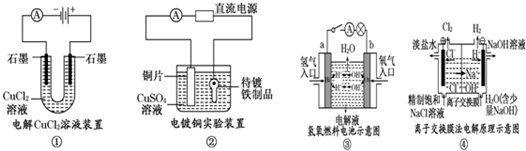

| A. | 装置①中阳极上析出红色固体 | |
| B. | 装置②的待镀铁制品应与电源负极相连 | |
| C. | 装置③中外电路电子由a极流向b极 | |
| D. | 装置④的阳极反应为:2H++2e-=H2↑ |
18.已知:H2、CO、CH4、C3H8 的燃烧热分别是285.8kJ/mol、283.0kJ/mol、890.3kJ/mol、2220.0kJ/mol,则等质量的这几种气体燃烧,产生热量最多的是( )
| A. | C3H8 | B. | CO | C. | H2 | D. | CH4 |
2.下列除杂试剂或操作方法不正确的是( )
| 选项 | 物质 | 杂质 | 除杂试剂或操作方法 |
| A | KNO3溶液 | KOH | 加入适量FeCl3溶液,过滤 |
| B | H2 | CO2 | 先后通过盛NaOH溶液、浓硫酸的洗气瓶 |
| C | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
| D | FeSO4溶液 | CuSO4 | 加入过量铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
3.某溶液中滴入BaCl2溶液,产生白色沉淀.再滴入稀硝酸,沉淀不溶解也无气体逸出,则该溶液中( )
| A. | 一定有SO42- | B. | 可能有Ag+或SO42- | ||
| C. | 一定无Ag+ | D. | 一定有CO32- |

 为探究亚硫酸钠的热稳定性,某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和下图所示的实验装置进行实验.请回答下列有关问题:
为探究亚硫酸钠的热稳定性,某研究性学习小组将无水亚硫酸钠隔绝空气加热,并利用受热后的固体试样和下图所示的实验装置进行实验.请回答下列有关问题: