题目内容
5.某种混合溶液中可能含有K+、CO32-、SO42-这些阴阳离子中的几种,某同学为了确定存在的阴、阳离子种类,设计了以下实验方案,请你帮该同学完成实验方案的内容:(1)取少量混合溶液于试管中,进行焰色反应,透过蓝色钴玻璃,如果观察到火焰呈紫色,证明溶液中含有K+.
(2)另取少量混合溶液,加入盐酸,若无明显现象,则说明不含有CO32-;再加入BaCl2溶液,若有产生白色沉淀,证明含有SO42-.
分析 K+、CO32-、SO42-中,可透过蓝色钴玻璃来检验K+,CO32-可与酸反应生成气体,加入盐酸酸化,再加入氯化钡可检验是否含有SO42-,以此解答该题.
解答 解:(1)证明溶液中含有K+,可透过蓝色钴玻璃来检验K+,观察到火焰呈紫色,故答案为:焰色反应; 蓝色钴玻璃;紫;
(2)CO32-可与酸反应生成气体,可先加入盐酸,若无明显现象,则说明不含有CO32-,再加入氯化钡可检验是否含有SO42-,
故答案为:盐酸;CO32-;BaCl2溶液.
点评 本题考查离子的检验,为高频考点,注意掌握离子反应发生条件,明确常见离子的化学性质为解答本题的关键,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
16.类比推理是化学中常用的思维方法.下列推理正确的是( )
| A. | Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3 | |
| B. | SiH4的沸点高于CH4,推测H2S的沸点高于H2O | |
| C. | CO2是直线型分子,推测CS2也是直线型分子 | |
| D. | NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr |
13.以下对电子转移的方向和数目的表示正确的是( )
| A. |  | B. |  | ||
| C. | 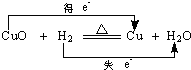 | D. |  |
20. 如图是一种验证某气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C处红色布条颜色无变化;当关闭B,继续通入Cl2时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
如图是一种验证某气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C处红色布条颜色无变化;当关闭B,继续通入Cl2时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
 如图是一种验证某气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C处红色布条颜色无变化;当关闭B,继续通入Cl2时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
如图是一种验证某气体化学性质的实验装置,图中B为开关.如先打开B,在A处通入干燥氯气,C处红色布条颜色无变化;当关闭B,继续通入Cl2时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )| A. | 浓H2SO4 | B. | 饱和NaCl溶液 | C. | NaOH溶液 | D. | Ca (OH) 2悬浊液 |
10.下列说法正确的是(NA为阿伏加德罗常数的值)( )
| A. | 1mol OH-与1mol-OH所含质子数均为9NA | |
| B. | pH=1的H2SO4溶液含H+的数目为0.2NA | |
| C. | 273K,101kPa条件下,14g乙烯与丙烯的混合物中含有的碳原子数目为3NA | |
| D. | 标准状况下,11.2L CCl4含有C-Cl键的数目为2NA |
17.下列各组离子在无色溶液中能够大量共存的是( )
| A. | NH4+、NO3-、Na+、SO42- | B. | H+、Fe3+、Na+、NO3- | ||
| C. | Ba2+、K+、Al3+、HCO3- | D. | NH4+、Li+、OH-、SO42- |
14.X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其他产物已略去):

下列说法不正确的是( )

下列说法不正确的是( )
| A. | 若W是单质铁,则Z溶液可能是FeCl2溶液 | |
| B. | 若W是盐酸,则X与Z可反应生成Y | |
| C. | 若X是FeCl3溶液,则W可以是Zn或Al | |
| D. | 若W是硝酸溶液,则X与Z不能反应生成Y |
15.铅蓄电池放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4↓+2H2O,根据此反应判断下列叙述中正确的是( )
| A. | Pb是电池的正极 | |
| B. | 负极的电极反应式为:Pb+SO42-+2e -=PbSO4↓ | |
| C. | PbO2得电子,被还原 | |
| D. | 电池充电时,溶液酸性减弱 |