题目内容
3.某溶液中滴入BaCl2溶液,产生白色沉淀.再滴入稀硝酸,沉淀不溶解也无气体逸出,则该溶液中( )| A. | 一定有SO42- | B. | 可能有Ag+或SO42- | ||
| C. | 一定无Ag+ | D. | 一定有CO32- |
分析 某溶液中加入BaCl2溶液生成白色沉淀,再加入稀硝酸沉淀不溶解也无气体逸出,生成的白色沉淀可能为氯化银或硫酸钡,溶液中可能含有硫酸根离子或银离子,以此解答该题.
解答 解:某溶液中加入BaCl2溶液生成白色沉淀,再加入稀硝酸沉淀不溶解也无气体逸出,说明溶液中不存在CO32-,生成的白色沉淀为硫酸钡或AgCl,原溶液中可能含有SO42-或Ag+,
故选B.
点评 本题考查了常见离子的检验方法,为高频考点,题目难度不大,明确常见离子的性质及检验方法为解答关键,注意判断离子是否存在时,必须排除干扰,确保检验方案的严密性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.以下对电子转移的方向和数目的表示正确的是( )
| A. |  | B. |  | ||
| C. | 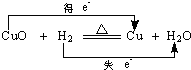 | D. |  |
14.X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其他产物已略去):

下列说法不正确的是( )

下列说法不正确的是( )
| A. | 若W是单质铁,则Z溶液可能是FeCl2溶液 | |
| B. | 若W是盐酸,则X与Z可反应生成Y | |
| C. | 若X是FeCl3溶液,则W可以是Zn或Al | |
| D. | 若W是硝酸溶液,则X与Z不能反应生成Y |
8.下列物质中,在标准状况下,体积最大的是( )
| A. | 8gH2 | B. | 48gO2 | C. | 71gCl2 | D. | 1000gH2O |
15.铅蓄电池放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4↓+2H2O,根据此反应判断下列叙述中正确的是( )
| A. | Pb是电池的正极 | |
| B. | 负极的电极反应式为:Pb+SO42-+2e -=PbSO4↓ | |
| C. | PbO2得电子,被还原 | |
| D. | 电池充电时,溶液酸性减弱 |
12.下列有关气体体积的描述中,正确的是( )
| A. | 一定温度和压强下,气体的体积主要由分子间的距离决定 | |
| B. | 通常状况下,气体摩尔体积约为22.4L | |
| C. | 标准状况下,气体摩尔体积约为22.4L | |
| D. | 单位物质的量的气体所占的体积就是气体摩尔体积 |
17.已知化学反应A2(g)+B2(g)?2AB(g)的能量变化如右图所示,判断下列叙述中正确的是( )


| A. | 该反应热△H=(a-b) kJ•mol-1 | |
| B. | 每生成2 mol AB(g)吸收b kJ能量 | |
| C. | 该反应中反应物的总能量高于生成物的总能量 | |
| D. | 断裂1 mol A-A和1 mol B-B键,放出a kJ能量 |