题目内容
1.除去下列物质中的杂质选用的试剂和方法最合理的是( )| 物质 | 杂质 | 试剂 | 方法 | |
| A | 二氧化碳 | 二氧化硫 | 饱和碳酸钠溶液 | 洗气 |
| B | 苯 | 苯酚 | 氢氧化钠溶液 | 分液 |
| C | 氯化钠溶液 | 碳酸钠 | 氨水、酒精 | 萃取、分液 |
| D | BaSO4 | BaCO3 | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二者均与碳酸钠溶液反应;
B.苯酚与NaOH溶液反应,与苯分层;
C.均不反应、不分层;
D.均不溶于水.
解答 解:A.二者均与碳酸钠溶液反应,不能除杂,应选饱和碳酸氢钠溶液,故A错误;
B.苯酚与NaOH溶液反应,与苯分层,然后分液可分离,故B正确;
C.均不反应、不分层,不能分液分离,故C错误;
D.均不溶于水,不能过滤分离,故D错误;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
11.科学家成功开发出便携式固体氧化物燃料电池,它以丙烷气体为燃料,空气为氧化剂,电解质是固态氧化物,在熔融状态下能传导O2-; 该电池的总反应是C3H8+5O2═3CO2+4H2O,负极反应为C3H8-20e-+10O2-═3CO2+4H2O.下列关于该燃料电池的说法中正确的是( )
| A. | 在熔融电解质中,O2-由负极移向正极 | |
| B. | 电池的正极通入丙烷 | |
| C. | 电路中每通过5 mol 电子,约有5.6 L标准状况下的丙烷被完全氧化 | |
| D. | 在电池正极的电极反应为O2-4e-═2O2- |
12.下列物质:①甲醇;②邻甲基苯酚;③甲醛;④甲酸;⑤甲酸钠;⑥甲酸甲酯,在一定条件下能与新制氢氧化铜悬浊液反应生成红色沉淀的是( )
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | 全部都可以 |
9.已知苯乙烯的结构为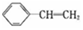 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )
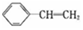 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )| A. | 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物有6种 | |
| B. | 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同 | |
| C. | 苯乙烯分子的所有原子不可能在同一平面上 | |
| D. | 除去 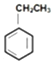 中的苯乙烯可以通入等量氢气反应 中的苯乙烯可以通入等量氢气反应 |
16.锂-二硫化亚铁电池是一种高容量电池,用途广泛,该电池放电时的总反应4Li+FeS2═Fe+2Li2S,下列说法正确的是( )
| A. | 放电时,负极反应为Li-e-═Li+ | |
| B. | 放电时,正极发生氧化反应 | |
| C. | 硫酸、羧酸及醇类物质都可以用作该锂电池的电解质 | |
| D. | 充电时,阳极只有Fe参与放电 |
6.向盛有不同试剂的试管b中分别滴加适量0.1mol/L FeCl3 溶液,下列对b中现象的解释正确的是( )
| 实验 | b中物质 | b中现象 | 结论或解释 | |
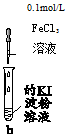 | A | Mg(OH)2悬浊液 | 有红棕色胶体产生 | 发生反应:Fe3++3OH-═Fe(OH)3(胶体) |
| B | Cu粉 | 溶液变蓝,试管底部有固体 | 溶液变蓝的原因是:3Cu+2Fe3+═2Fe+3Cu2+ | |
| C | 5%H2O2溶液 | 有气泡生成 | 该气体为氯气,双氧水强氧化性氧化Cl-产生 | |
| D | 饱和NaHCO3溶液 | 有气泡生成,且试管底部有固体 | 发生反应:Fe3++3HCO3-═Fe(OH)3+3CO2 |
| A. | A | B. | B | C. | C | D. | D |
13.下列物质的水溶液因水解显酸性的是( )
| A. | CH3COONa | B. | KCl | C. | NaHSO4 | D. | NH4Cl |
20.元素周期律和周期表揭示了元素之间的内在联系,反映了元素性质与它的原子结构的关系.下列有关性质的大小关系符合元素周期律的是( )
| A. | 酸性:HNO3>H3BO3>H2CO3 | B. | 稳定性:HF>PH3>H2O | ||
| C. | 碱性:Be(OH)2>Mg(OH)2>Ca(OH)2 | D. | 金属性:K>Mg>Al |
 乙酸乙酯是非常重要的有机溶剂和化工原料,如图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品.请回答:
乙酸乙酯是非常重要的有机溶剂和化工原料,如图转化关系中的①、②、③是工业上合成乙酸乙酯的常见反应,其中A是一种常见的调味品.请回答: