题目内容
16.锂-二硫化亚铁电池是一种高容量电池,用途广泛,该电池放电时的总反应4Li+FeS2═Fe+2Li2S,下列说法正确的是( )| A. | 放电时,负极反应为Li-e-═Li+ | |
| B. | 放电时,正极发生氧化反应 | |
| C. | 硫酸、羧酸及醇类物质都可以用作该锂电池的电解质 | |
| D. | 充电时,阳极只有Fe参与放电 |
分析 A、放电时负极发生氧化反应;
B、放电时正极发生还原反应;
C、加入硫酸、羧酸时,Li和硫酸、羧酸反应;
D、充电时,阳极发生氧化反应,而反应中S和Fe的化合价都升高.
解答 解:A、放电时负极发生氧化反应,电极反应式为:Li-e-═Li+,故A正确;
B、放电时正极发生还原反应,而不是还原反应,故B错误;
C、加入硫酸、羧酸时,Li和硫酸、羧酸反应,所以不能用硫酸、羧酸及醇类物质用作该锂电池的电解质,故C错误;
D、充电时,阳极发生氧化反应,而反应中S和Fe的化合价都升高,所以S和Fe参与放电,故D错误;
故选A.
点评 本题考查化学电源新型电池,侧重考查原电池和电解池原理,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,要注意题干中电解质特点,为易错点.

练习册系列答案
相关题目
7.下列各组离子可能大量共存的是( )
| A. | 常温下,c(H+)=1×10-12mol•L-1的溶液中:A13+、Fe3+、SO42-、Cl- | |
| B. | pH=0的溶液中:Fe2+、Ba2+、NO3-、Cl- | |
| C. | 常温下,水电离的c(H+)为1×10-12mol•L-1的溶液中:Na+、NH4+、HCO3-、NO3- | |
| D. | 能使酚酞试液变红色的溶液中:Na+、K+、SiO32-、S2O32- |
4.下列有关性质的比较,不能用元素周期律解释的是( )
| A. | 碱性:KOH>NaOH | B. | 金属性:Na>Al | C. | 稳定性:HF>CH4 | D. | 酸性:HClO<HClO4 |
11.已知LiAl/FeS电池是一种新型的车载电池,对该电池充电时,阳极的电极反应式为:Li2S+Fe-2e-=2Li++FeS.下列有关该电池的说法中,正确的是( )
| A. | 化合物LiAl具有强还原性,作负极材料 | |
| B. | 为了延长电池的使用寿命,可以隔一段时间添加含电解质的水溶液 | |
| C. | 放电时,该电池的总反应式为2Li+FeS═Li2S+Fe | |
| D. | 放电时,当电路中0.1mol电子的电量时,有0.1molLi+向LiAl移动 |
1.除去下列物质中的杂质选用的试剂和方法最合理的是( )
| 物质 | 杂质 | 试剂 | 方法 | |
| A | 二氧化碳 | 二氧化硫 | 饱和碳酸钠溶液 | 洗气 |
| B | 苯 | 苯酚 | 氢氧化钠溶液 | 分液 |
| C | 氯化钠溶液 | 碳酸钠 | 氨水、酒精 | 萃取、分液 |
| D | BaSO4 | BaCO3 | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
8. “天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.如图图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )
“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.如图图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )
 “天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.如图图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )
“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将太阳能电池电解水技术与氢氧燃料电池技术相结合的可充电电池.如图图为RFC工作原理示意图(隔膜为质子选择性透过膜),下列说法中正确的是( )| A. | RFC系统工作过程中只存在3种形式的能量转化 | |
| B. | 装置I与装置II的电解质溶液中,氢离子运动方向相反 | |
| C. | c极上发生的电极反应是:O2+4H++4e-=2H2O | |
| D. | 当有0.1mol电子转移时,b极产生1.12L 气体Y(标准状况下) |
5.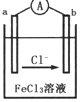 某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )
某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )
 某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )
某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )| A. | Zn为负极,发生还原反应 | |
| B. | b电极反应式为ZFe3++2e-═2Fe2+ | |
| C. | 电子流动方向是a电极→FeCl3溶液→b电极 | |
| D. | 电池的正极材料可以选用石墨、铂电极,也可以用铜电极 |
15.25℃时,下列溶液中的微粒浓度关系正确的是( )
| A. | pH=3的0.1mol•L-1的NaHC2O4溶液中:c(C2O42-)<c(H2C2O4) | |
| B. | 0.1mol•L-1的Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) | |
| C. | pH=4的CH3COOH溶液中:$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-10 | |
| D. | 等物质的量浓度、等体积的NaF溶液和HF溶液混合所得的稀溶液中:c(H+)+c(Na+)=c(F-)+c(OH-) |