题目内容
10.0.01mol有机物A 在氧气中完全燃烧生成2.2gCO2和1.08gH2O,无其它物质生成.试回答下列问题:(1)若A为烃,则A的分子式为C5H12;若它的一卤代物有4种,此烃的结构简式为:
 .用系统法命名为:2-甲基丁烷.
.用系统法命名为:2-甲基丁烷.(2)若A为一元醇且不能被氧气催化氧化.则A的键线式为
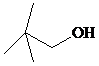 ,其名称(系统法命名)为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成H2的体积为11.2L(标况)
,其名称(系统法命名)为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成H2的体积为11.2L(标况)
分析 n(CO2)=$\frac{2.2g}{44g/mol}$=0.05mol,n(H2O)=$\frac{1.08g}{18g/mol}$=0.06mol,则1mol有机物含有5molC、12molH,
(1)若A为烃,则A的分子式为C5H12,若它的一卤代物有4种,说明含有4种不同的H原子,应为2-甲基丁烷;
(2)若A为一元醇且不能被氧气催化氧化,说明连接羟基的碳原子上没有H原子.
解答 解:n(CO2)=$\frac{2.2g}{44g/mol}$=0.05mol,n(H2O)=$\frac{1.08g}{18g/mol}$=0.06mol,则1mol有机物含有5molC、12molH,
(1)若A为烃,则A的分子式为C5H12,若它的一卤代物有4种,说明含有4种不同的H原子,应为2-甲基丁烷,结构简式为 ,
,
故答案为:C5H12; ;2-甲基丁烷;
;2-甲基丁烷;
(2)若A为一元醇且不能被氧气催化氧化,说明连接羟基的碳原子上没有H原子,应为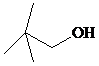 ,为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成0.5mol氢气,在标准状况下的体积为11.2L,
,为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成0.5mol氢气,在标准状况下的体积为11.2L,
故答案为: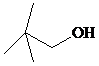 ;2,2-二甲基-1-丙醇;11.2.
;2,2-二甲基-1-丙醇;11.2.
点评 本题考查了有机物分子式的确定、有机物的命名等知识,侧重学生的分析、计算能力的考查,题目难度中等,注意掌握确定有机物分子式、结构简式的方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.已知锌能溶解在NaOH溶液中,产生H2.某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6mol/L NaOH溶液中,当石墨棒上不再有气泡产生时,取出铁片用水冲洗、烘干后称量,得质量为m2.下列说法正确的是( )
| A. | 设锌镀层厚度为h,锌的密度为ρ,则$\frac{{{m_1}-{m_2}}}{ρS}$=h | |
| B. | 锌电极上发生还原反应 | |
| C. | 锌和石墨形成原电池,外电路中电流从锌流向石墨 | |
| D. | 当石墨不再产生气泡时,应立即取出铁皮 |
1.短周期主族元素X、Y、Z、W的原子序数依次增大,其原子的最外层电子数之和为19.X的简单阴离子比W的简单阴离子少2层电子,Y与Z位于相邻周期,Z的氧化物排放到空气中会形成酸雨.下列说法正确的是( )
| A. | 四种元素中,元素Z的非金属性最强 | |
| B. | X、Y、Z三种元素不可能形成离子化合物 | |
| C. | Y、Z、W三种元素的原子半径大小顺序:r(W)>r(Z)>r(Y) | |
| D. | YW3、ZW2、Z2W2中各原子最外层均达到8电子稳定结构 |
5.下列不属于有机物的是( )
| A. | 氯化钠 | B. | 醋酸 | C. | 乙炔 | D. | 尿素 |
15.在共价化合物中元素化合价有正负,其主要原因是( )
| A. | 电子有得失 | B. | 共用电子对有偏移 | ||
| C. | 电子既有得失又有电子对偏移 | D. | 含有多种非金属元素 |
2.用氯丙醛(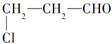 )制取聚丙烯酸(
)制取聚丙烯酸(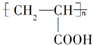 )的过程中发生的反应类型为( )
)的过程中发生的反应类型为( )
①取代 ②消去 ③加聚 ④还原 ⑤氧化.
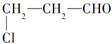 )制取聚丙烯酸(
)制取聚丙烯酸(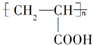 )的过程中发生的反应类型为( )
)的过程中发生的反应类型为( )①取代 ②消去 ③加聚 ④还原 ⑤氧化.
| A. | ⑤①②③ | B. | ⑤②③ | C. | ①②⑤③ | D. | ②③⑤④ |
19.对于放热反应Zn+H2SO4═ZnSO4+H2↑,下列叙述正确的是( )
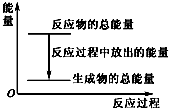

| A. | 反应过程中的能量关系可用如图表示 | |
| B. | 1 mol Zn的能量大于1 mol H2的能量 | |
| C. | 若将其设计为原电池,则锌作正极 | |
| D. | 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L |
