题目内容
20.已知锌能溶解在NaOH溶液中,产生H2.某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6mol/L NaOH溶液中,当石墨棒上不再有气泡产生时,取出铁片用水冲洗、烘干后称量,得质量为m2.下列说法正确的是( )| A. | 设锌镀层厚度为h,锌的密度为ρ,则$\frac{{{m_1}-{m_2}}}{ρS}$=h | |
| B. | 锌电极上发生还原反应 | |
| C. | 锌和石墨形成原电池,外电路中电流从锌流向石墨 | |
| D. | 当石墨不再产生气泡时,应立即取出铁皮 |
分析 A、根据面积等于质量比密度,厚度等于面积比表面积判断;
B、锌是电源的负极发生氧化反应;
C、电子由负极沿导线正极,而电流刚好相反;
D、如果石墨不再产生气泡时,说明锌已完全反应.
解答 解:A、面积等于质量比密度,厚度等于面积比表面积,设锌镀层为h,锌的密度为ρ,则h=$\frac{{m}_{1}-{m}_{2}}{2ρS}$,故A错误;
B、锌能溶解在NaOH溶液中,产生H2,所以锌是电源的负极发生氧化反应,故B错误;
C、电子由负极沿导线正极,所以电流由正极石墨流向负极锌,故C错误;
D、如果石墨不再产生气泡时,说明锌已完全反应,取出铁皮除去表面杂质,然后称重,故D正确;
故选D.
点评 本题考查原电池工作原理,电极反应的类型和电流的流向,比较容易.

练习册系列答案
相关题目
10.已知Ksp(AgCl)=1.8×10-10;Ksp(AgBr)=5.3×10-13,将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,发生的反应为( )
| A. | AgCl沉淀多于AgBr沉淀 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | 只有AgBr沉淀生成 |
11.已知3Fe3O4+28HNO3(稀)═9Fe(NO3)3+14H2O+NO↑下列说法正确的是( )
| A. | Fe3O4是氧化剂,Fe2+是还原剂 | |
| B. | 每生成1mol NO,则转移电子数为2mol | |
| C. | 参加反应的氧化剂与还原剂的物质的最之比为28:3 | |
| D. | 若有3mol Fe3O4被氧化,则被还原的HNO3为1mol |
8.关于原电池和电解池的叙述,正确的是( )
| A. | 电解池的阳极,原电池负极都发生还原反应 | |
| B. | 不能自发进行的氧化还原反应,通过电解的原理可以实现 | |
| C. | 原电池的两极,一定要由活泼性不同的两种金属组成 | |
| D. | 电解池中阳离子移向阴极,原电池中阳离子移向负极 |
15.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A、容器中压强不变 B、混合气体中c(CO)不变
C、混合气体的密度不变 D、c(CO)=c(CO2)
E、化学平衡常数K不变 F、单位时间内生成CO的分子数与生成H2O的分子数相等
(4)某温度下,各物质的平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A、容器中压强不变 B、混合气体中c(CO)不变
C、混合气体的密度不变 D、c(CO)=c(CO2)
E、化学平衡常数K不变 F、单位时间内生成CO的分子数与生成H2O的分子数相等
(4)某温度下,各物质的平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
5.若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物:(1)CH3Cl,(2)CH2Cl2,(3)CHCl3,(4)CCl4,(5)HCl其中正确的是( )
| A. | 只有(1)(5) | B. | 只有(3)(5) | C. | (1)(2)(3)(5)的混合物 | D. | (1)(2)(3)(4)(5)的混合物 |
9.对于某些离子的检验及结论一定正确的是( )
| A. | 通入Cl2后,溶液变为黄色,加淀粉液后溶液变蓝,则原溶液中一定有I- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定有SO42- | |
| C. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
 CH3COOCH2CH3+H2O,该反应的类型为取代反应.
CH3COOCH2CH3+H2O,该反应的类型为取代反应. .用系统法命名为:2-甲基丁烷.
.用系统法命名为:2-甲基丁烷.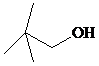 ,其名称(系统法命名)为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成H2的体积为11.2L(标况)
,其名称(系统法命名)为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成H2的体积为11.2L(标况)