题目内容
15.按要求书写方程式:(1)写出氯化铵与氢氧化钠溶液共热的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(2)写出钠与水反应的化学方程式2H2O+2Na=2OH-+H2↑+2Na+.
(3)写出碳酸氢钠受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
分析 (1)反应生成氯化钠、氨气、水;
(2)反应生成NaOH和氢气;
(3)碳酸氢钠分解生成碳酸钠、水、二氧化碳.
解答 解:(1)反应生成氯化钠、氨气、水,离子反应为NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,故答案为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;
(2)反应生成NaOH和氢气,化学反应为2H2O+2Na=2OH-+H2↑+2Na+,故答案为:2H2O+2Na=2OH-+H2↑+2Na+;
(3)碳酸氢钠分解生成碳酸钠、水、二氧化碳,反应为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
点评 本题考查离子反应方程式及化学反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
5.将过量SO2通入下列溶液中,能出现白色浑浊的是( )
①Ca(OH)2
②BaCl2
③NaAlO2
④Na2SiO3
⑤Ba(NO3)2
⑥苯酚钠
⑦Na2CO3.
①Ca(OH)2
②BaCl2
③NaAlO2
④Na2SiO3
⑤Ba(NO3)2
⑥苯酚钠
⑦Na2CO3.
| A. | ①②④⑦ | B. | ②③⑥⑦ | C. | ④⑤⑥⑦ | D. | ③④⑤⑥ |
3.下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2反应
②Fe与过量稀H2SO4反应
③Fe和Fe2O3的混合物溶于盐酸中.
①过量的Fe与Cl2反应
②Fe与过量稀H2SO4反应
③Fe和Fe2O3的混合物溶于盐酸中.
| A. | 只有① | B. | ①② | C. | ①②③ | D. | ①③ |
10.下列反应中氯元素既被氧化又被还原的是( )
| A. | 5Cl2+I2+6H2O═10HCl+2HIO3 | |
| B. | 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | |
| C. | MnO2+4HCl═MnCl2+2H2O+Cl2↑ | |
| D. | 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑ |
20.下列说法正确的是( )
| A. | 制备硫酸亚铁晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液被全部蒸干 | |
| B. | 向1 mL浓度均为0.05 mol•L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol•L-1的AgNO3溶液,振荡,沉淀呈黄色.结论:Ksp(AgCl)<Ksp(AgI) | |
| C. | 常温下,将CH3COONa、HCl两溶液混合后,溶液呈中性,溶液中c(Na+)大于c(Cl-) | |
| D. | pH相等的下列溶液:a.CH3COOK、b.NaHCO3、c.Na2CO3、d.NaOH,其物质的量浓度由小到大顺序 为:d<c<a<b |
4.下列实验现象中有白烟出现的是( )
| A. | 铜丝在Cl2中燃烧 | B. | 铁丝在氧气中燃烧 | ||
| C. | 氢气在氯气中燃烧 | D. | Na在Cl2中燃烧 |
5.下列关于乙酸的说法正确的是( )
| A. | 常温下是一种无色无味的气体 | B. | 能和乙醇发生加成反应 | ||
| C. | 能和Na2CO3溶液反应 | D. | 能使紫色石蕊试液变蓝 |
 实验室里若用如图所示装置制取氨气,试用表格形式列出图中装置的错误之处,并用文字简要说明如何改正.
实验室里若用如图所示装置制取氨气,试用表格形式列出图中装置的错误之处,并用文字简要说明如何改正. ,芳香族化合物乙与甲互为同分异构体,能与NaOH溶液反应,但不能使FeCl3溶液显紫色,写出乙与NaOH溶液反应的化学方程式:
,芳香族化合物乙与甲互为同分异构体,能与NaOH溶液反应,但不能使FeCl3溶液显紫色,写出乙与NaOH溶液反应的化学方程式: +2NaOH$\stackrel{△}{→}$HCOONa+
+2NaOH$\stackrel{△}{→}$HCOONa+ +H2O.
+H2O.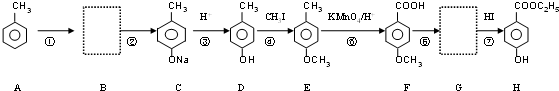
 .反应⑥的试剂和条件是乙醇、浓H2SO4.加热不能与H反应的物质是a.(选填字母)
.反应⑥的试剂和条件是乙醇、浓H2SO4.加热不能与H反应的物质是a.(选填字母)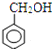 或
或 .
. .
.