题目内容
18.下列关于苯乙烯(结构简式为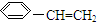 )的叙述错误的是( )
)的叙述错误的是( )| A. | 可以和溴水反应 | |
| B. | 分子中所有原子可能共面 | |
| C. | 是苯的同系物 | |
| D. | 1mol苯乙烯可以和4mol H2发生加成反应 |
分析 苯乙烯含有一个个碳碳双键,具有烯烃的性质,结合苯、乙烯的结构和性质解答该题.
解答 解:A.苯环上连接的碳碳双键易发生加成反应,可以和溴水反应,故A正确;
B.含有苯环和碳碳双键,都为平面形结构,则分子中所有原子可能共面,故B正确;
C.含有碳碳双键,与苯的结构不同,不是同系物,故C错误;
D.苯环在一定条件下能发生加成反应,苯环上连接的碳碳双键易发生加成反应,1摩尔苯乙烯能与4摩尔氢气发生加成反应,故D正确.
故选C.
点评 本题考查有机物的结构与性质,注意把握有机物中的官能团,熟悉烯烃、苯醇的性质即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列除杂质的操作方法正确的是( )
| A. | NO中有少量的NO2:用水洗涤后再干燥 | |
| B. | 食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干 | |
| C. | O2中有少量的CO:通过灼热的氧化铜 | |
| D. | NO2中有少量NH3:用水洗涤后干燥 |
8.实验室制备乙酸乙酯和乙酸丁酯采用的相同措施是( )
| A. | 水浴加热 | B. | 冷凝回流 | ||
| C. | 用浓硫酸做脱水剂和催化剂 | D. | 乙酸过量 |
6.已知H-H键能为436kJ/mol,H-N键能为391kJ/mol,N≡N键的键能为946kJ/mol,则反应:N2(g)+3H2(g)═2NH3(g)△H=?( )
| A. | +46 kJ/mol | B. | +92kJ/mol | C. | -46 kJ/mol | D. | -92 kJ/mol |
13.下列有机物,不能溶于水的是( )
| A. | 酒精 | B. | 醋酸 | C. | 乙醛 | D. | 硝基苯 |
3.化学与材料、生活和环境密切相关.下列有关说法中错误的是( )
| A. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| B. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| C. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 | |
| D. | 石英、玛瑙的主要成分是二氧化硅,陶瓷、分子筛主要成分是硅酸盐 |
10.表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na;
(2)最高价氧化物的水化物碱性最强的化合物是NaOH,酸性最强的化合物是HClO4,呈两性的化合物是Al(OH)3;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HF;
(4)在B、C、D、E、F、G、H中,原子半径最大的是Na.
(5)写出E的单质的结构式N≡N:
(6)写出BG组成的化合物的形成过程 :
:
| 族周期 | ⅠA | 0 | ||||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的化合物是NaOH,酸性最强的化合物是HClO4,呈两性的化合物是Al(OH)3;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HF;
(4)在B、C、D、E、F、G、H中,原子半径最大的是Na.
(5)写出E的单质的结构式N≡N:
(6)写出BG组成的化合物的形成过程
 :
:
7.惰性电极电解下列溶液一段时间,加入一定质量的另一种物质(括号内),溶液可以完全复原的是( )
| A. | NaOH(NaOH) | B. | NaCl(HCl) | C. | CuCl2 (CuO) | D. | H2SO4 (H2SO4 ) |
8.某同学利用如图装置探究SO2的性质.
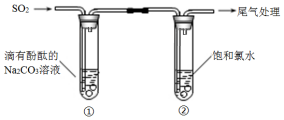
下列有关反应的方程式,不正确的是( )

下列有关反应的方程式,不正确的是( )
| A. | ①中溶液显红色的原因:CO32-+H2O?HCO3-+OH- | |
| B. | ①中溶液红色褪去的原因:2SO2+CO32-+H2O═CO2+2HSO3- | |
| C. | ②中溶液显黄绿色的原因:Cl2+H2O═HCl+HClO | |
| D. | ②中溶液黄绿色褪去的原因:SO2+Cl2+2H2O═H2SO4+2HCl |