题目内容
19.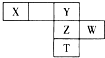 如图下表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X的最高正价与最低负价绝对值只差等于0.下列说法正确的是( )
如图下表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X的最高正价与最低负价绝对值只差等于0.下列说法正确的是( )| A. | X氢化物的沸点一定比Y氢化物的沸点低 | |
| B. | T的最高价氧化物对应的水化物酸性比Z的强 | |
| C. | Y的氢化物沸点高于Z的氢化物,因为H-Y键的键能高于H-Z键 | |
| D. | XY2、XZ2、XW4的化学键类型相同、晶体类型也相同 |
分析 X的最高正价与最低负价绝对值只差等于0,X应为ⅣA族元素,应为C,由元素在周期表中的位置可知Y为O元素,Z为S元素,T为Se元素,W为Cl元素,结合元素对应单质、化合物的性质以及元素周期率的相似性和递变性解答该题.
解答 解:X的最高正价与最低负价绝对值只差等于0,X应为ⅣA族元素,应为C,由元素在周期表中的位置可知Y为O元素,Z为S元素,T为Se元素,W为Cl元素,
A.水含有氢键,沸点较高,故A错误;
B.同主族元素从上到下元素的非金属性逐渐减弱,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,T的最高价氧化物对应的水化物酸性比Z的弱,故B错误;
C.Y的氢化物沸点高于Z的氢化物,是由于水含有氢键,与共价键无关,故C错误;
D.XY2、XZ2、XW4的化学键类型都为极性共价键,且都为分子晶体,故D正确.
故选D.
点评 本题考查了元素周期表和元素周期律的应用,题目难度中等,合理推断各元素为解答关键,注意熟练掌握元素周期表结构、元素周期律内容,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
9.下列有关物质结构的说法中,正确的是( )
| A. | CO2和SiO2都是直线形分子 | |
| B. | H2O和NH3的VSEPR模型不同 | |
| C. | 由分子构成的物质中一定含有共价键 | |
| D. | 形成共价键的元素不一定是非金属元素 |
10.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 64g Cu粉与足量硫粉加热完全反应生成Cu2S时失去的电子数为2NA | |
| B. | 足量的CO2与39gNa2O2发生反应转移的电子数为NA | |
| C. | 18g的D2O与NA个-CH3具有相同的电子数 | |
| D. | 6.0g醋酸晶体中含有H+的数目为0.1NA |
7.利用酸性含锰废水(主要锰废水(主要含Mn2+、Cl-、H+、Fe2+、Cu2+)可制备高性能磁性材料碳酸锰(Mn)纯净的氯化铜晶体(CuCl2•2H2O).工业流程如下:
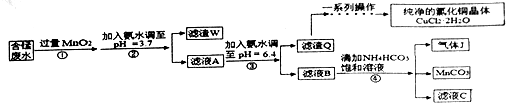
已知某些物质完全沉淀的pH值如下表
回答下列问题:
(1)过程①中,MnO2在酸性条件下可将Fe2+氧化为Fe3+,反应的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O.
(2)过程②中,所得滤渣W的成分是Fe(OH)3和过量的MnO2.
(3)过程③中,调pH=6.4目的是使Cu2+ 完全沉淀为Cu(OH)2.
(4)过程④中,若生成的气体J可使澄清石灰水变浑浊,则生成MnCO3反应的离子方程式是Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(5)将滤渣Q溶解在过量的盐酸中,经过加热浓缩,降温结晶,过滤、洗涤、低温烘干,即可获得纯净的氯化钠晶体(CuCl2•2H2O).
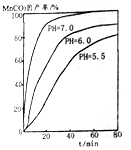
(6)过程④中,298K、c(Mn2+)为1.05mol•L-1时,实验测得MnCO3的产率与溶液pH、反应时间关系如图所示,据图中信息,你选择的最佳pH是7.0;理由是pH等于7.0时反应速率最快,且MnCO3产率最高.
(7)从滤液C可得到的副产品是NH4Cl(填化学式).

已知某些物质完全沉淀的pH值如下表
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 沉淀完全的pH | 9.7 | 3.7 | 6.4 | 10.4 |
(1)过程①中,MnO2在酸性条件下可将Fe2+氧化为Fe3+,反应的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O.
(2)过程②中,所得滤渣W的成分是Fe(OH)3和过量的MnO2.
(3)过程③中,调pH=6.4目的是使Cu2+ 完全沉淀为Cu(OH)2.
(4)过程④中,若生成的气体J可使澄清石灰水变浑浊,则生成MnCO3反应的离子方程式是Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(5)将滤渣Q溶解在过量的盐酸中,经过加热浓缩,降温结晶,过滤、洗涤、低温烘干,即可获得纯净的氯化钠晶体(CuCl2•2H2O).
(6)过程④中,298K、c(Mn2+)为1.05mol•L-1时,实验测得MnCO3的产率与溶液pH、反应时间关系如图所示,据图中信息,你选择的最佳pH是7.0;理由是pH等于7.0时反应速率最快,且MnCO3产率最高.

(7)从滤液C可得到的副产品是NH4Cl(填化学式).
14.短周期主族元素W、X、Y、Z的原子序数依次增大,W的一种单质是自然界中最硬的物质,工业上采用分馏液态空气的方法来生产X的单质,且X单质化学性质不活泼,Y、Z阴离子的核外电子数与氩原子电子数相同,且Y原子最外层电子数是其电子层数的2倍.下列有关该四种元素说法正确的是( )
| A. | 原子半径大小为W>X>Z>Y | |
| B. | X、Y、Z的氢化物的水溶液均呈酸性 | |
| C. | W与Y形成的三原子化合物既含极性共价键又含非极性共价键 | |
| D. | Z元素的最高价氧化物对应的水化物酸性最强 |
11.化学与环境、生活密切相关,下列与化学有关的说法正确的是( )
| A. | 春节燃放爆竹对环境无污染 | |
| B. | “酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 家庭用的“84”消毒液与洁厕灵可同时混合使用 |
8.化学与人类生活密切相关,下列与化学有关的说法正确的是( )
| A. | 化学药品着火,都要立即用水或泡沫灭火器灭火 | |
| B. | 明矾和漂白粉常用于自来水的净化,但两者的作用原理不相同 | |
| C. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 | |
| D. | 纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 |
9.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 形成化学键 | B. | 氢气燃烧 | C. | 铝热反应 | D. | 电解熔融氯化钠 |
 .
.