题目内容
17.把下列溶液加水稀释,溶液的PH值不会改变的是( )| A. | CH3COOH溶液 | B. | NaCl溶液 | C. | NaOH溶液 | D. | FeCl3溶液 |
分析 酸性溶液稀释pH会增大,碱性溶液稀释pH会减小,中性溶液稀释pH不变,据此分析.
解答 解:A.CH3COOH溶液加水稀释,溶液中氢离子浓度减小,pH增大,故A不选;
B.NaCl溶液显中性,加水稀释pH不变,故B选;
C.NaOH溶液加水稀释,溶液中氢氧根离子浓度减小,pH减小,故C不选;
D.FeCl3溶液显酸性,加水稀释,溶液中氢离子浓度减小,pH增大,故D不选.
故选B.
点评 本题考查了溶液pH的变化,题目难度不大,注意把握加水稀释对溶液酸碱性的影响,侧重于考查学生的分析能力.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
18.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 沸点高的物质制备沸点低的物质 | 钙置换出铷,或浓磷酸制备HI |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | BCl3沸点低于AlCl3,CO2沸点低于SiO2 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | AgCl沉淀中滴加NaI溶液,会得到AgI沉淀 |
| A. | A | B. | B | C. | C | D. | D |
2.常温下,下列有关醋酸溶液的叙述中不正确的是( )
| A. | pH=4.3的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) | |
| B. | 浓度为0.2 mol/L的CH3COOH溶液和浓度为0.1 mol/L的NaOH溶液等体积混合后:c(CH3COO -)-c(CH3COOH)=2[c(H+)-c(OH -)] | |
| C. | 醋酸浓溶液加少量水稀释,$\frac{c(C{H}_{3}COOH)}{{c}^{2}({H}^{+})}$几乎不变 | |
| D. | a mol/L CH3COOH溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)>c(CH3COO-),则一定有a≤b |
9.某酸溶液的pH=1,此酸溶液的物质的量浓度( )
| A. | 0.1 mol•L-1 | |
| B. | 一定大于0.1 mol•L-1 | |
| C. | 若为强酸一定等于0.1 mol•L-1,若为弱酸一定小于0.1 mol•L-1 | |
| D. | 若为强酸一定≤0.1 mol•L-1,若为弱酸一定>0.1 mol•L-1 |
6.升高温度,下列溶液的pH不发生变化的是( )
| A. | 0.05mol•L-1的H2SO4 | B. | 0.1mol•L-1的KNO3 | ||
| C. | 0.1mol•L-1的KOH | D. | 0.1mol•L-1的NH4NO3 |
7.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由苯硝化制硝基苯;由乙醇氧化制乙醛 | |
| C. | 由乙酸和乙醇制乙酸乙酯;由乙酸乙酯水解制乙醇 | |
| D. | 由氯代乙烷制乙烯;由丙烯制1,2-二溴丙烷 |
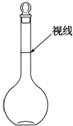 实验室配制480mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有:
实验室配制480mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有: