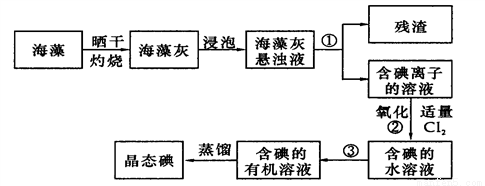
��Ŀ����
����40��ǰ����ѧ��ʦHeilbronner���������о�Ԥ�⣬Ӧ���п��ܺϳɡ�Ī����˹����״�ķ�����(��)��ϩ���ӣ���һԤ�ⱻ�¹���ѧ�Һϳ�֤ʵ��[18]-��ϩ��һ�ִ���ϩ����ṹ��ʽ��ͼ��ʾ�� �й�����˵����ȷ����
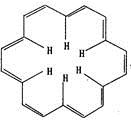
A. [18]- ��ϩ����������ԭ�Ӳ����ܴ���ͬһƽ��
B. [18]- ��ϩ�ķ���ʽΪ��C18H12
C. 1 mol[18]- ��ϩ������9 mol���������ӳɷ�Ӧ���ɻ�����
D. [18]- ��ϩ����ϩ��Ϊͬϵ�
 ������������ϵ�д�
������������ϵ�д���1����֪25 ��ʱ�й�����ĵ���ƽ�ⳣ����
���ữѧʽ | HSCN | CH3COOH | HCN | H2CO3 |
����ƽ�ⳣ�� | 1.3��10-1 | 1.8��10-5 | 4.9��10-10 | K1=4.3��10-7 K2=5.6��10-11 |
�� ͬ�¶��£���pHֵ��a. NaHCO3��b. NaCN��c��Na2CO3��Һ�����ʵ���Ũ���ɴ�С��˳��Ϊ__________������ţ���
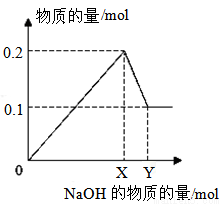
�� 25 ��ʱ����20mL 0.1mol/LCH3COOH��Һ��20mL0.1mol/LHSCN��Һ�ֱ���20ml0.1mol/L NaHCO3��Һ��ϣ�ʵ���ò������������(V)��ʱ��(t)�ı仯��ͼ��ʾ��

��Ӧ��ʼ��������Һ����CO2��������ʴ������Բ����ԭ���ǣ�________��Ӧ��������������Һ�У�c(SCN-)________c(CH3COO-)���> ������< ����= ��)
�� �������¶Ȳ��䣬�ڴ�����Һ�м���һ�������������������С����______������ţ���
a.c(CH3COO-�� b.c(H+) c.Kw d���������ƽ�ⳣ��
��2��úȼ�ղ���������Ҳ�������������CH4����ԭNOx�������������������Ⱦ����֪��CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ��H=-867.0kJ mol-1
2NO2(g) N2O4(g) ��H=-56.9kJ mol-1
N2O4(g) ��H=-56.9kJ mol-1
H2O(g)=H2O(l) ��H=-44.0kJ mol-1
д��CH4����ԭN2O4(g������N2(g)��CO2(g)��H2O(l)���Ȼ�ѧ����ʽ_________
��3������ȼ�ϵ�ؿ����������������ʡ���ͼ�����ü���ȼ�ϵ�ص��50mL 2mol/L���Ȼ�ͭ��Һ��װ��ʾ��ͼ����ش��������⣺

�ټ���ȼ�ϵ�صĸ�����Ӧʽ��____________
�� ��A������0.15mol����ʱ��B ��____������_______g��



 �� �����ʣ�Ϊ����Ч��ȥCa2+��Mg2+��SO
�� �����ʣ�Ϊ����Ч��ȥCa2+��Mg2+��SO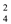 �����������ӱ��Լ����ñ��Լ�������___________��
�����������ӱ��Լ����ñ��Լ�������___________��