题目内容
某课外活动小组对银镜反应中影响出现银镜时间的因素和银镜的处理方法进行了探究.
I、影响银镜出现时间的因素探究:请观察表,回答问题:
(1)同学们进行实验1、2、4和5,其目的是 ;若当银氨溶液量为1ml,乙醛溶液量为3滴,反应混合液PH为11,水浴温度为55℃时,推测出现银镜的时间为 ;
(2)同学们为探究乙醛用量对出现银镜时间的影响,进行的实验是 ;
(3)按该小组预设的影响因素,没有完成实验探究的影响因素是 、 ;若要探究这些因素对出现银镜快慢的影响,还应如何设计实验? ;
II、银镜处理方法探究:
活动小组同学认为传统的用稀硝酸溶解银镜后再回收银的方法存在较大缺点.他们通过查阅资料,设计探究实验:实验1:取15ml 10% H2O2溶液倒入附有银镜的试管中.现象:银镜溶解,同时产生无色气体.为进一步探究反应产物,进行实验2…3…,(略)同学们通过实验现象,最终得出结论:H2O2溶液可以溶解银镜,在反应后得到单质银.
(4)写出传统的稀硝酸溶解银镜的化学方程式并标出电子转移方向和数目: ;
(5)用H2O2溶液处理银镜与稀硝酸处理银镜相比,其优点为 (写出一点即可);
(6)猜想实验1中产生的气体为 ,检验方法为 .
I、影响银镜出现时间的因素探究:请观察表,回答问题:
| 实验变量 实验序号 | 银氨溶液量 (ml) | 乙醛的量 (滴) | 水浴温度 (℃) | 反应混合液PH | 出现银镜时间(min) |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
(2)同学们为探究乙醛用量对出现银镜时间的影响,进行的实验是
(3)按该小组预设的影响因素,没有完成实验探究的影响因素是
II、银镜处理方法探究:
活动小组同学认为传统的用稀硝酸溶解银镜后再回收银的方法存在较大缺点.他们通过查阅资料,设计探究实验:实验1:取15ml 10% H2O2溶液倒入附有银镜的试管中.现象:银镜溶解,同时产生无色气体.为进一步探究反应产物,进行实验2…3…,(略)同学们通过实验现象,最终得出结论:H2O2溶液可以溶解银镜,在反应后得到单质银.
(4)写出传统的稀硝酸溶解银镜的化学方程式并标出电子转移方向和数目:
(5)用H2O2溶液处理银镜与稀硝酸处理银镜相比,其优点为
(6)猜想实验1中产生的气体为
考点:乙醛的银镜反应
专题:实验设计题
分析:(1)对比实验:实验1、2、4和5的反应条件,其它条件相同,只有水浴温度不同;其它条件相同,随着温度升高,反应速率加快:其它条件相同,温度为55℃时的反应速率应该在温度为50℃温度为65℃之间;
(2)对比实验:实验1和实验3的反应条件,其它条件相同,只有乙醛的用量不同;
(3)要想探索银氨溶液的用量或溶液PH值对出现银镜快慢的影响,设计对比实验;
(4)根据反应方程式,结合化合价升降结合电子转移方向解答;
(5)根据产物是否含有有害气体进行判断;
(6)猜想实验1中产生的气体为O2或H2,根据猜想气体的性质进行验证;
(2)对比实验:实验1和实验3的反应条件,其它条件相同,只有乙醛的用量不同;
(3)要想探索银氨溶液的用量或溶液PH值对出现银镜快慢的影响,设计对比实验;
(4)根据反应方程式,结合化合价升降结合电子转移方向解答;
(5)根据产物是否含有有害气体进行判断;
(6)猜想实验1中产生的气体为O2或H2,根据猜想气体的性质进行验证;
解答:
解:(1)对比实验:实验1、2、4和5的反应条件,其它条件相同,只有水浴温度不同,其实验目的是:探究水浴温度对出现银镜时间的影响,由实验1和实验5知:银氨溶液的量为1mL,乙醛的量为3滴,反应混合液pH为11时,水浴温度为50℃,出现银镜时间为6min,水浴温度为65℃,出现银镜时间为5min,其它条件相同,随着温度升高,反应速率加快,故:当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为55℃,反应混合液pH为11时,出现银镜的时间应在5min到6min之间;
故答案为:探究水浴温度对出现银镜时间的影响; 在5-6分钟之间;
(2)对比实验1和实验3的反应条件,其它条件相同,只有乙醛的用量不同,其实验目的是:比较银镜反应中,乙醛用量不同对生成银镜的影响;
故答案为:实验1和3;
(3)要想探索银氨溶液的用量对出现银镜快慢的影响,需设计对比实验:银氨溶液的用量不同,保持乙醛的量、水液温度、反应混合液的PH相同,测量比较生成银镜的时间,或保持银氨溶液的用量相同,乙醛的量、水液温度相同、改变PH值,
故答案为:银氨溶液量和pH值,保持其他实验条件相同,改变银氨溶液量或溶液PH值,分别测定出现银镜时间;
(4)在反应3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O中,银元素的化合价由0升高到+1价,N元素的化合价由+5降低为+2价,转移的电子为3e-,
则双线桥法标出电子得失的方向和数目为: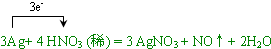 ,
,
故答案为: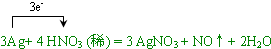 ;
;
(5)银和稀硝酸反应,方程式为:3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O,用稀硝酸溶解样品会生成NO,NO是有毒气体,会污染环境,用双氧水溶解银,不会产生有害气体,
故答案为:无有害气体产生,不污染环境;反应后产物Ag易集中回收;
(6)猜想过氧化氢银作用生成氢气或氧气,将带火星的木条至于试管口,若木条复燃,则为O2,反之为H2,
故答案为:O2或H2;将带火星的木条至于试管口,若木条复燃,则为O2,反之为H2;
故答案为:探究水浴温度对出现银镜时间的影响; 在5-6分钟之间;
(2)对比实验1和实验3的反应条件,其它条件相同,只有乙醛的用量不同,其实验目的是:比较银镜反应中,乙醛用量不同对生成银镜的影响;
故答案为:实验1和3;
(3)要想探索银氨溶液的用量对出现银镜快慢的影响,需设计对比实验:银氨溶液的用量不同,保持乙醛的量、水液温度、反应混合液的PH相同,测量比较生成银镜的时间,或保持银氨溶液的用量相同,乙醛的量、水液温度相同、改变PH值,
故答案为:银氨溶液量和pH值,保持其他实验条件相同,改变银氨溶液量或溶液PH值,分别测定出现银镜时间;
(4)在反应3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O中,银元素的化合价由0升高到+1价,N元素的化合价由+5降低为+2价,转移的电子为3e-,
则双线桥法标出电子得失的方向和数目为:
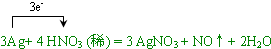 ,
,故答案为:
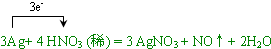 ;
;(5)银和稀硝酸反应,方程式为:3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O,用稀硝酸溶解样品会生成NO,NO是有毒气体,会污染环境,用双氧水溶解银,不会产生有害气体,
故答案为:无有害气体产生,不污染环境;反应后产物Ag易集中回收;
(6)猜想过氧化氢银作用生成氢气或氧气,将带火星的木条至于试管口,若木条复燃,则为O2,反之为H2,
故答案为:O2或H2;将带火星的木条至于试管口,若木条复燃,则为O2,反之为H2;
点评:本题考查了对比实验的要求和方法,银镜反应的条件和及方程式的书写,以及Ag和过氧化氢、稀HNO3反应比较,题目难度中等,掌握实验探究的方法和银镜反应的原理是解答的关键.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
在理论上不能用于设计原电池的化学反应是( )
| A、2FeCl3(aq)+2KI(aq)═2FeCl2(aq)+2KCl(aq)+I2(aq)△H<0 |
| B、Ba(OH)2?8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3?H2O(aq)+8H2O(l)△H>0 |
| C、4Al(s)+6H2O(l)+3O2(g)═4Al(OH)3(s)△H<0 |
| D、Zn(s)+2MnO2(s)+2H2O(l)═2MnOOH(s)+Zn(OH)2(s)△H<0 |
如图是元素周期表短周期的一部分.其中F原子的电子层数为n,最外层电子数为2n+1,核内质子数为2n2-1.下列说法不正确的是( )
| A | B | C | |
| D | E | F |
| A、D的单质是常见的半导体材料 |
| B、B与E形成的化合物不只一种 |
| C、C与F的原子序数之差一定为8 |
| D、C属于卤族元素,对应的单质能与水反应生成两种酸 |
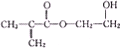 甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )
甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )| A、能发生加成反应 |
| B、能发生取代反应 |
| C、一定条件下,能与乙醇发生酯化反应 |
| D、既能是溴水褪色,又能使酸性高猛酸钾溶液褪色 |

 下面的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,B为液体,C能使湿润的红色石蕊试纸变蓝.A、B、C的物质的量之比为1:1:1.
下面的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,B为液体,C能使湿润的红色石蕊试纸变蓝.A、B、C的物质的量之比为1:1:1.