题目内容
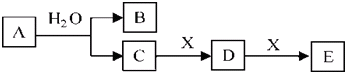
10.如图中 A、B、C、D、E均为有机化合物.已知:A的分子式为C14H18O4,C能跟NaHCO3发生反应,C和D的相对分子质量相等,E为无支链的链状化合物.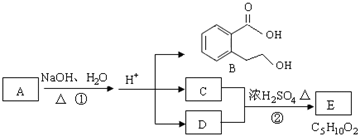
根据图回答问题:
(1)化合物B不能发生的反应是e(填序号).
a.加成反应 b.取代反应 c.消去反应 d.酯化反应 e.水解反应 f.置换反应
(2)反应②的化学方程式是CH3COOH+CH3CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH3+H2O.
(3)A的结构简式是
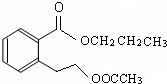 或
或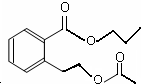 .
.(4)同时符合下列三个条件的B的同分异构体的数目有4个;
Ⅰ含有间二取代苯环结构Ⅱ属于非芳香酸形成的酯Ⅲ与FeCl3溶液发生显色反应.
写出其中任意一个同分异构体的结构简式
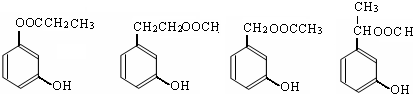 .
.
分析 C能跟NaHCO3发生反应,说明C含有羧基,C和D的相对分子质量相等,E的分子式为C5H10O2,且E为无支链的化合物,E为CH3COOCH2CH2CH3,C为CH3COOH、D为CH3CH2CH2OH,A水解然后酸化得到B、乙酸和丙醇,则A结构简式为 或
或 ,以此解答该题.
,以此解答该题.
解答 解:(1)有机物B中含有醇羟基、羧基和苯环,具有醇、羧酸和苯的性质,能发生加成反应、氧化反应、取代反应、酯化反应、消去反应、置换反应,因为不含氯原子或酯基,所以不能发生水解反应,故答案为:e;
(2)丙醇和乙酸发生酯化反应生成乙酸丙酯,反应方程式为CH3COOH+CH3CH2CH2OH$?_{△}^{浓硫酸}$ CH3COOCH2CH2CH3+H2O,
故答案为:CH3COOH+CH3CH2CH2OH$?_{△}^{浓硫酸}$ CH3COOCH2CH2CH3+H2O;
(3)通过以上分析知,A的结构简式为 或
或 ,
,
故答案为: 或
或 ;
;
(4)B的同分异构体符合下列条件:
Ⅰ.含有间二取代苯环结构;
Ⅱ.属于非芳香酸酯,说明不是苯酸形成的酯;
Ⅲ.与 FeCl3 溶液发生显色反应,说明含有酚羟基,
反应条件的同分异构体有 ,所以有4种符合条件的,
,所以有4种符合条件的,
故答案为:4;  .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,正确判断E结构简式是解本题关键,采用逆向思维方法进行推断,难点是(4)题同分异构体种类判断.

练习册系列答案
相关题目
19.下列关于有机化合物的说法正确的是( )
| A. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物数目不相同 | |
| B. | 乙烷,苯,葡萄糖溶液均不能使酸性高锰酸钾溶液褪色 | |
| C. | 苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环己烷的密度都比水大 | |
| D. | 与环己醇( )互为同分异构体、且含有醛基(-CHO)的结构有8种(不含立体结构) )互为同分异构体、且含有醛基(-CHO)的结构有8种(不含立体结构) |
20.下列关于有机物的说法正确的是( )
| A. | 糖类、油脂、蛋白质在一定条件下均能水解 | |
| B. | 乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物 | |
| C. | 分子式为C4H8C12的有机物共有(不含立体异构)8种 | |
| D. | 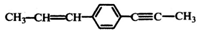 处于同一平面上的原子数最多为18个 处于同一平面上的原子数最多为18个 |
17.下列有关实验操作设计、现象记录、结论解释都正确的是( )
| 实验操作设计 | 现象记录 | 结论解释 | |
| A | 醋酸加入到碳酸钠固体中,将产生的气体通入C6H5ONa 溶液中 | 溶液变浑浊 | 酸性:CH3COOH>H2CO3>C6H5OH |
| B | CH3CH2Br 与NaOH 乙醇溶液共热产生的气体通入溴水中 | 溶液褪色 | 产生了乙烯 |
| C | 向某氯化亚铁溶液中加入加入Na2O2 粉末 | 出现红褐色沉淀 | 加入 Na2O2 粉末前,原氯化亚铁溶液已经变质 |
| D | 向紫色石蕊试液中持续长时 间通人氯气 | 溶液先变红,最后变为无色 | 氯气有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
5.下列反应中,属于吸热反应的是( )
| A. | 氢气在在氯气中燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | CaCO3与稀盐酸反应制取CO2 | D. | CaO溶于水 |
15.已知下列化合物:①硝基苯 ②环己烷 ③乙苯 ④溴苯 ⑤间二硝基苯.其中能由苯通过一步反应直接制取的是( )
| A. | ①②③ | B. | ①③⑤ | C. | ①②④ | D. | 全部 |
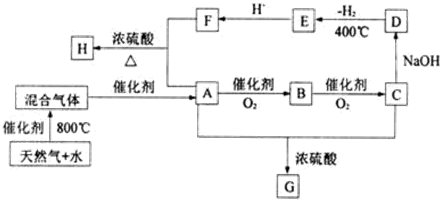
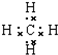 ;E的化学式是Na2C2O4.
;E的化学式是Na2C2O4.