题目内容
已知0.1mol有机物A的质量是12g,在足量的氧气中充分燃烧后生成0.8mol CO2和7.2g H2O;A可以发生银镜反应,其苯环上的一卤代物有三种.已知:

现有如下转化关系:
其中D能使溴的四氯化碳溶液褪色,F继续被氧化生成G,G的相对分子质量为90.
(1)A的分子式是 ,A中含氧官能团的名称是 ,A的结构简式为 .
(2)C可能具有的化学性质有 (填序号).
①能与H2发生加成反应 ②能在碱性溶液中发生水解反应 ③能与甲酸发生酯化反应④能与Ag(NH3)2OH溶液发生银镜反应
(3)①写出C→D的化学反应方程式 ;②一定条件下,D生成高聚物的化学方程式 ;
③G与NaHCO3溶液反应的化学方程式 .
(4)向盛有5mL G饱和溶液的试管中滴入3滴用稀硫酸酸化的KMnO4溶液,振荡,观察到的现象是 ,说明G具有 性.
(5)C的同分异构体有多种,其中符合下列要求的有机物有两种:
①属于酯类化合物 ②遇三氯化铁溶液显紫色 ③与新制氢氧化铜悬浊液共热可生成红色沉淀 ④苯环上的一卤代物只有一种写出其中一种有机物的结构简式 .

现有如下转化关系:

其中D能使溴的四氯化碳溶液褪色,F继续被氧化生成G,G的相对分子质量为90.
(1)A的分子式是
(2)C可能具有的化学性质有
①能与H2发生加成反应 ②能在碱性溶液中发生水解反应 ③能与甲酸发生酯化反应④能与Ag(NH3)2OH溶液发生银镜反应
(3)①写出C→D的化学反应方程式
③G与NaHCO3溶液反应的化学方程式
(4)向盛有5mL G饱和溶液的试管中滴入3滴用稀硫酸酸化的KMnO4溶液,振荡,观察到的现象是
(5)C的同分异构体有多种,其中符合下列要求的有机物有两种:
①属于酯类化合物 ②遇三氯化铁溶液显紫色 ③与新制氢氧化铜悬浊液共热可生成红色沉淀 ④苯环上的一卤代物只有一种写出其中一种有机物的结构简式
考点:有机物的合成
专题:有机物的化学性质及推断
分析:0.1mol有机物A的质量是12g,则Mr(A)=12÷0.1=120,0.1molA在足量的氧气中充分燃烧后生成0.8molCO2和7.2g H2O,根据原子守恒可知,该有机物中N(C)=
=8、N(H)=
=8,故有机物中N(O)=
=1,故有机物的分子式为C8H8O,A可以发生银镜反应,含有醛基-CHO,苯环上的一卤代物有三种,苯环上有3种化学环境不同的H原子,故只能有1个侧链为-CH2CHO,则A的结构简式为 ,由信息Ⅰ可知,A与HCN发生加成反应生成B为
,由信息Ⅰ可知,A与HCN发生加成反应生成B为 ,B发生水解反应生成C为
,B发生水解反应生成C为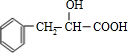 ,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为
,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为 ,
, 发生氧化反应生成E与F,由信息Ⅱ可知氧化为
发生氧化反应生成E与F,由信息Ⅱ可知氧化为 、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为
、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为 ,G为HOOC-COOH,据此解答.
,G为HOOC-COOH,据此解答.
| 0.8mol |
| 0.1mol |
| ||
| 0.1mol |
| 120-12×8-8 |
| 16 |
 ,由信息Ⅰ可知,A与HCN发生加成反应生成B为
,由信息Ⅰ可知,A与HCN发生加成反应生成B为 ,B发生水解反应生成C为
,B发生水解反应生成C为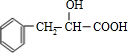 ,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为
,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为 ,
, 发生氧化反应生成E与F,由信息Ⅱ可知氧化为
发生氧化反应生成E与F,由信息Ⅱ可知氧化为 、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为
、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为 ,G为HOOC-COOH,据此解答.
,G为HOOC-COOH,据此解答.解答:
解:0.1mol有机物A的质量是12g,则Mr(A)=12÷0.1=120,0.1molA在足量的氧气中充分燃烧后生成0.8molCO2和7.2g H2O,根据原子守恒可知,该有机物中N(C)=
=8、N(H)=
=8,故有机物中N(O)=
=1,故有机物的分子式为C8H8O,A可以发生银镜反应,含有醛基-CHO,苯环上的一卤代物有三种,苯环上有3种化学环境不同的H原子,故只能有1个侧链为-CH2CHO,则A的结构简式为 ,由信息Ⅰ可知,A与HCN发生加成反应生成B为
,由信息Ⅰ可知,A与HCN发生加成反应生成B为 ,B发生水解反应生成C为
,B发生水解反应生成C为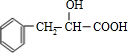 ,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为
,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为 ,
, 发生氧化反应生成E与F,由信息Ⅱ可知氧化为
发生氧化反应生成E与F,由信息Ⅱ可知氧化为 、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为
、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为 ,G为HOOC-COOH,
,G为HOOC-COOH,
(1)A为 ,分子式为C8H8O,含氧官能团的名称是醛基,
,分子式为C8H8O,含氧官能团的名称是醛基,
故答案为:C8H8O;醛基; ;
;
(2)C为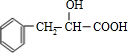 ,含有苯环,可以与氢气发生加成反应,含有羟基,可以与甲酸发生酯化反应,含有羧基,能与氢氧化钠发生中和反应,不能发生水解反应,不能与银氨溶液反应,
,含有苯环,可以与氢气发生加成反应,含有羟基,可以与甲酸发生酯化反应,含有羧基,能与氢氧化钠发生中和反应,不能发生水解反应,不能与银氨溶液反应,
故选:①③;
(3)①C→D的化学反应方程式为 ;
;
②D为 ,在催化剂条件下,生成高聚物的化学方程式为n
,在催化剂条件下,生成高聚物的化学方程式为n
 ;
;
③G与足量NaHCO3溶液反应的化学方程式为: ,
,
故答案为: ;n
;n
 ;
; ;
;
(4)G为HOOC-COOH,向盛有5mL G饱和溶液的试管中滴入3滴用稀硫酸酸化的KMnO4溶液,振荡,观察到高锰酸钾溶液紫色褪去,说明G具有还原性,
故答案为:高锰酸钾溶液紫色褪去;还原;
(5)C(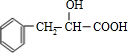 )的同分异构体有多种,符合下列条件的同分异构体:
)的同分异构体有多种,符合下列条件的同分异构体:
①属于酯类化合物;②遇三氯化铁溶液显紫色,含有酚羟基;③与新制氢氧化铜悬浊液共热可生成红色沉淀,含有甲酸形成的酯基,④苯环上的一卤代物只有一种,符合条件的同分异构体有: ,
,
故答案为: ;
;
| 0.8mol |
| 0.1mol |
| ||
| 0.1mol |
| 120-12×8-8 |
| 16 |
 ,由信息Ⅰ可知,A与HCN发生加成反应生成B为
,由信息Ⅰ可知,A与HCN发生加成反应生成B为 ,B发生水解反应生成C为
,B发生水解反应生成C为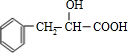 ,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为
,C在浓硫酸、加热条件下生成D,D能使溴的四氯化碳溶液褪色,应为发生消去反应,故D为 ,
, 发生氧化反应生成E与F,由信息Ⅱ可知氧化为
发生氧化反应生成E与F,由信息Ⅱ可知氧化为 、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为
、OHC-COOH,F继续被氧化生成G,G的相对分子质量为90,故F为OHC-COOH,E为 ,G为HOOC-COOH,
,G为HOOC-COOH,(1)A为
 ,分子式为C8H8O,含氧官能团的名称是醛基,
,分子式为C8H8O,含氧官能团的名称是醛基,故答案为:C8H8O;醛基;
 ;
;(2)C为
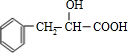 ,含有苯环,可以与氢气发生加成反应,含有羟基,可以与甲酸发生酯化反应,含有羧基,能与氢氧化钠发生中和反应,不能发生水解反应,不能与银氨溶液反应,
,含有苯环,可以与氢气发生加成反应,含有羟基,可以与甲酸发生酯化反应,含有羧基,能与氢氧化钠发生中和反应,不能发生水解反应,不能与银氨溶液反应,故选:①③;
(3)①C→D的化学反应方程式为
 ;
;②D为
 ,在催化剂条件下,生成高聚物的化学方程式为n
,在催化剂条件下,生成高聚物的化学方程式为n
| 催化剂 |
 ;
;③G与足量NaHCO3溶液反应的化学方程式为:
 ,
,故答案为:
 ;n
;n
| 催化剂 |
 ;
; ;
;(4)G为HOOC-COOH,向盛有5mL G饱和溶液的试管中滴入3滴用稀硫酸酸化的KMnO4溶液,振荡,观察到高锰酸钾溶液紫色褪去,说明G具有还原性,
故答案为:高锰酸钾溶液紫色褪去;还原;
(5)C(
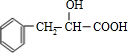 )的同分异构体有多种,符合下列条件的同分异构体:
)的同分异构体有多种,符合下列条件的同分异构体:①属于酯类化合物;②遇三氯化铁溶液显紫色,含有酚羟基;③与新制氢氧化铜悬浊液共热可生成红色沉淀,含有甲酸形成的酯基,④苯环上的一卤代物只有一种,符合条件的同分异构体有:
 ,
,故答案为:
 ;
;
点评:本题考查有机物推断与性质,是对有机化合物知识的综合考查,能较好的考查考生的自学能力,读懂信息中给予的反应是解题的关键,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液.相同条件下,有关上述溶液的比较中,不正确的是( )
| A、水电离的c(H+):①=②=③=④ |
| B、若将②、③溶液混合后,pH=7,则消耗溶液的体积:②=③ |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:①最大 |
| D、向溶液中加入100mL水后,溶液的pH:③>④>②>① |




 有多种同分异构体,写出同分异构体中所有含有1个醛基和2个羟基的芳香族化合物的结构简式
有多种同分异构体,写出同分异构体中所有含有1个醛基和2个羟基的芳香族化合物的结构简式
