题目内容
“C 1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH、HCOOH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.相关数据如下:
请回答:
①a= .
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是 mol?L-1?S-1.
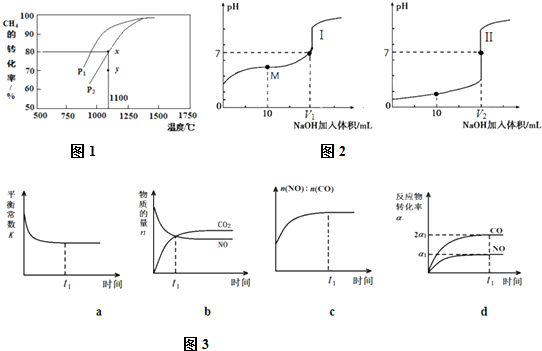
(2)甲烷的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)?2CO(g)+2H2(g)在密闭容器中通入等物质的量浓度的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图1所示,则压强P1 P2(填“大于”或“小于”);压强为P2时,在y点:v(正) v(逆)(填“大于”、“小于”或“等于”).
(3)一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.在恒温恒容的密闭容器中通入n(NO):n(CO)=2:1的混合气体,发生上述反应.下列图象如图3正确且能说明反应在进行到t1时刻一定达到平衡状态的是 (选填字母).
(4)甲酸(HCOOH)是一种弱酸,现用0.1mol?L-1 NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol?L-1的盐酸和甲酸溶液,滴定曲线如图2:
滴定开始前,三种溶液中由水电离出的c(H+)最大的是 ;V1和V2的关系V1 V2(填
“>”、“=”或“<”);M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 .

(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.相关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
①a=
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是
(2)甲烷的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)?2CO(g)+2H2(g)在密闭容器中通入等物质的量浓度的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图1所示,则压强P1
(3)一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.在恒温恒容的密闭容器中通入n(NO):n(CO)=2:1的混合气体,发生上述反应.下列图象如图3正确且能说明反应在进行到t1时刻一定达到平衡状态的是
(4)甲酸(HCOOH)是一种弱酸,现用0.1mol?L-1 NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol?L-1的盐酸和甲酸溶液,滴定曲线如图2:
滴定开始前,三种溶液中由水电离出的c(H+)最大的是
“>”、“=”或“<”);M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是
考点:化学平衡的计算,化学平衡的影响因素,化学平衡状态的判断,酸碱混合时的定性判断及有关ph的计算
专题:
分析:(1)①A、B是等效平衡,则A中放出的热量与B中吸收的热量之和为49.0kJ;
②平衡时能量变化放出29.4kJ,求平衡时各组分的浓度,然后求平均反应速率;
(2)该反应正向为体积增大的方向,压强越大,CH4的转化率越小;压强为P2时,在Y点反应未达到平衡,则反应正向移动;
(3)可逆反应达到平衡状态时,正逆反应速率相等,各组分浓度不再变化,据此进行判断.
(4)酸和碱都对水的电离起抑制作用,酸、碱性越强,水的电离程度越小;甲酸钠显示碱性,氯化钠显示中性;0.1mol?L-1 NaOH溶液10mL和溶液体积为20.00mL0.1mol?L-1的甲酸反应,得到的是甲酸和甲酸钠的混合物,据此确定离子浓度大小.
②平衡时能量变化放出29.4kJ,求平衡时各组分的浓度,然后求平均反应速率;
(2)该反应正向为体积增大的方向,压强越大,CH4的转化率越小;压强为P2时,在Y点反应未达到平衡,则反应正向移动;
(3)可逆反应达到平衡状态时,正逆反应速率相等,各组分浓度不再变化,据此进行判断.
(4)酸和碱都对水的电离起抑制作用,酸、碱性越强,水的电离程度越小;甲酸钠显示碱性,氯化钠显示中性;0.1mol?L-1 NaOH溶液10mL和溶液体积为20.00mL0.1mol?L-1的甲酸反应,得到的是甲酸和甲酸钠的混合物,据此确定离子浓度大小.
解答:
解:(1)①甲、乙是等效平衡,则甲中放出的热量与乙中吸收的热量之和为49.0kJ,则a=49.0kJ-29.4kJ=19.6kJ,故答案为:19.6;
②平衡时能量变化放出29.4kJ,所以反应二氧化碳的物质的量为
=0.6mol,所以,然后求平均反应速率v=
=0.03mol/(L?min),故答案为:0.03;
(2)该反应正向为体积增大的方向,压强越大,CH4的转化率越小,已知相同温度下,P1条件下的转化率大于P2,则P1小于P2;压强为P2时,在Y点反应未达到平衡,则反应正向移动,所以v(正)大于v(逆);
故答案为:小于;大于;
(3)当反应前后改变的物理量不变时,该可逆反应达到平衡状态,
a中为平衡常数,平衡常数与温度有关,温度不变,则平衡常数始终不变,所以平衡常数不能判断是否达到平衡状态,故a错误;
b为物质的量随时间的变化,一氧化氮与二氧化碳浓度相等时,各组分浓度仍然继续变化,说明没有达到平衡状态,故b错误;
c为CO质量分数随时间变化,反应恰好总质量不变,则反应过程中一氧化氮与一氧化碳的物质的量之比会发生变化,当达到平衡状态时,一氧化氮与一氧化碳的物质的量之比不再变化,故c正确;
d、反应物的转化率不变,说明达平衡状态,故d正确;
故答案为:cd;
(4)0.1mol?L-1 NaOH溶液、0.1mol?L-1的盐酸中氢离子和氢氧根浓度都是0.1mol/L,对水的抑制作用一样,但是0.1mol/L甲酸溶液中氢离子浓度小于0.1mol/L,所以对水的电离抑制较小,即三种溶液中由水电离出的c(H+)最大的是0.1 mol?L-1甲酸溶液;根据图象中两线的起点可知,Ⅰ线甲酸溶液,Ⅱ线为盐酸溶液,甲酸和氢氧化钠之间的反应,当恰好完全反应得到的甲酸钠显示碱性,要使得溶液显示中性,pH=7,需要甲酸稍过量,所以盐酸和氢氧化钠恰好完全反应,得到的氯化钠显示中性,所以V1<V2;用0.1mol?L-1 NaOH溶液10mL和溶液体积为20.00mL0.1mol?L-1的甲酸反应,得到的是甲酸和甲酸钠的混合物,显示酸性,此时离子浓度大小c(HCOO-)>c (Na+)>c (H+)>c (OH-),
故答案为:甲酸溶液;<;c(HCOO-)>c (Na+)>c (H+)>c (OH-).
②平衡时能量变化放出29.4kJ,所以反应二氧化碳的物质的量为
| 29.4kJ |
| 49.0kJ |
| ||
| 10s |
(2)该反应正向为体积增大的方向,压强越大,CH4的转化率越小,已知相同温度下,P1条件下的转化率大于P2,则P1小于P2;压强为P2时,在Y点反应未达到平衡,则反应正向移动,所以v(正)大于v(逆);
故答案为:小于;大于;
(3)当反应前后改变的物理量不变时,该可逆反应达到平衡状态,
a中为平衡常数,平衡常数与温度有关,温度不变,则平衡常数始终不变,所以平衡常数不能判断是否达到平衡状态,故a错误;
b为物质的量随时间的变化,一氧化氮与二氧化碳浓度相等时,各组分浓度仍然继续变化,说明没有达到平衡状态,故b错误;
c为CO质量分数随时间变化,反应恰好总质量不变,则反应过程中一氧化氮与一氧化碳的物质的量之比会发生变化,当达到平衡状态时,一氧化氮与一氧化碳的物质的量之比不再变化,故c正确;
d、反应物的转化率不变,说明达平衡状态,故d正确;
故答案为:cd;
(4)0.1mol?L-1 NaOH溶液、0.1mol?L-1的盐酸中氢离子和氢氧根浓度都是0.1mol/L,对水的抑制作用一样,但是0.1mol/L甲酸溶液中氢离子浓度小于0.1mol/L,所以对水的电离抑制较小,即三种溶液中由水电离出的c(H+)最大的是0.1 mol?L-1甲酸溶液;根据图象中两线的起点可知,Ⅰ线甲酸溶液,Ⅱ线为盐酸溶液,甲酸和氢氧化钠之间的反应,当恰好完全反应得到的甲酸钠显示碱性,要使得溶液显示中性,pH=7,需要甲酸稍过量,所以盐酸和氢氧化钠恰好完全反应,得到的氯化钠显示中性,所以V1<V2;用0.1mol?L-1 NaOH溶液10mL和溶液体积为20.00mL0.1mol?L-1的甲酸反应,得到的是甲酸和甲酸钠的混合物,显示酸性,此时离子浓度大小c(HCOO-)>c (Na+)>c (H+)>c (OH-),
故答案为:甲酸溶液;<;c(HCOO-)>c (Na+)>c (H+)>c (OH-).
点评:本题考查了热化学方程式和盖斯定律的计算应用、酸碱滴定、弱电解质的电离和盐类的水解、化学平衡状态的判断等,涉及的知识点较多,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
构成下列四种物质的微粒间,既存在离子键又存在共价键的是( )
| A、NH4Cl |
| B、K2S |
| C、MgCl2 |
| D、SO3 |
下列化学用语正确的是( )
A、K+离子的结构示意图: |
B、四氯化碳的电子式: |
C、CH4分子的比例模型: |
| D、次氯酸的结构式:H-O-Cl |
下列变化属于化学变化的是( )
| A、过滤法除去水中的泥沙 |
| B、分液法分离汽油与水 |
| C、蒸馏法除去酒精中的水 |
| D、沉淀法除去钠离子中的钙离子 |
用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、28gCO和N2的混合气体中含有原子总数为2NA |
| B、常温常压下,2g氢气所含原子数目为2NA |
| C、标准状况下,足量Fe与22.4LCl2反应,转移电子数为2NA |
| D、0.1mol/LNa2CO3溶液中含有的Na+数目为0.2NA |




