题目内容
5.以下离子检验正确的是( )| A. | 检验试液中的SO42-:试液$\stackrel{BaCl_{2}溶液}{→}$ 白色沉淀$\stackrel{HCl溶液}{→}$ 白色沉淀 | |
| B. | 检验试液中的Cl-:试液$\stackrel{稀H_{2}SO_{4}}{→}$无沉淀$\stackrel{AgNO_{3}溶液}{→}$ 白色沉淀 | |
| C. | 检验试液中的Fe2+:试液$\stackrel{氯水}{→}$无明显现象$\stackrel{KSCN溶液}{→}$血红色溶液 | |
| D. | 检验试液中的NH4+:试液$→_{供热}^{NaOH溶液}$气体逸出$→_{石蕊试纸}^{湿润的红色}$ 试纸变蓝 |
分析 A.检验硫酸根离子,先加盐酸排除干扰离子;
B.检验氯离子,先加硝酸酸化,排除干扰离子;
C.检验亚铁离子,先加KSCN溶液,无现象,再加氯水;
D.铵根离子与碱反应生成氨气,氨气使红色石蕊试纸变蓝.
解答 解:A.检验硫酸根离子,先加盐酸排除干扰离子,试剂加入顺序不合理,不能检验,故A错误;
B.检验氯离子,先加硝酸酸化,排除干扰离子,试剂不合理,硫酸银为白色沉淀干扰氯离子检验,故B错误;
C.检验亚铁离子,先加KSCN溶液,无现象,再加氯水,溶液为血红色,试剂顺序不合理,故C错误;
D.铵根离子与碱反应生成氨气,氨气使红色石蕊试纸变蓝,检验方法合理,故D正确;
故选D.
点评 本题考查常见离子的检验,为高频考点,把握检验试剂、试剂顺序、现象与结论的关系为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.有200mL氯化镁和氯化铝混合液,其中c(Mg2+)为0.2mol•L-1,c(Cl-)为1.3mol•L-1,要使沉淀量达最大值,需加4mol•L-1NaOH溶液的体积为( )
| A. | 20mL | B. | 45mL | C. | 65mL | D. | 80mL |
10.实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液.
(2)容量瓶上需标有以下五项中的①③⑤.
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是BCAFED(用字母表示,每个字母只能用一次).
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶,溶液注入容量瓶前需恢复到室温,这是因为容量瓶盛放热溶液时,体积不准.
(5)下列配制的溶液浓度偏小的是ABEF.
A.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
B.加蒸馏水时不慎超过了刻度线、
C.定容时俯视刻度线
D.配制前,容量瓶中有少量蒸馏水.
E.称量NaOH时,砝码错放在左盘
F.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水.
(1)配制250mL 1.25mol/L的NaOH溶液.
| 应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外,还需要的其它玻璃仪器 |
| 12.5g | 250mL | 烧杯、玻璃棒、胶头滴管 |
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是BCAFED(用字母表示,每个字母只能用一次).
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶,溶液注入容量瓶前需恢复到室温,这是因为容量瓶盛放热溶液时,体积不准.
(5)下列配制的溶液浓度偏小的是ABEF.
A.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
B.加蒸馏水时不慎超过了刻度线、
C.定容时俯视刻度线
D.配制前,容量瓶中有少量蒸馏水.
E.称量NaOH时,砝码错放在左盘
F.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水.
14.以强制弱是物质世界的普遍规律.已知:四种物质的氧化能力Cl2>Br2>FeCl3>I2,下列氧化还原反应不能发生的是( )
| A. | 2I-+Cl2═I2+2Cl- | B. | 2Br-+Cl2═Br2+2Cl- | ||
| C. | Br2+2I-═2Br-+I2 | D. | 2Fe2++I2═2Fe3++2I- |
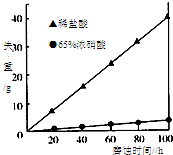 按要求回答下列问题:
按要求回答下列问题: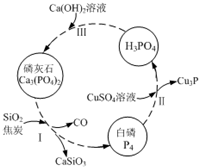 氮、磷及其化合物在科研及生产中均有着重要的应用.
氮、磷及其化合物在科研及生产中均有着重要的应用.