题目内容
14.以强制弱是物质世界的普遍规律.已知:四种物质的氧化能力Cl2>Br2>FeCl3>I2,下列氧化还原反应不能发生的是( )| A. | 2I-+Cl2═I2+2Cl- | B. | 2Br-+Cl2═Br2+2Cl- | ||
| C. | Br2+2I-═2Br-+I2 | D. | 2Fe2++I2═2Fe3++2I- |
分析 根据化学方程式,只要根据氧化还原反应中还原剂的还原性强于还原产物的还原性,氧化剂的氧化性强于氧化产物的氧化性得出的结果符合题干已知条件的,说明反应成立.
解答 解:A、根据2I-+Cl2═I2+2Cl-可知氧化性是Cl2>I2,符合题干已知条件,所以化学方程式成立,故A正确;
B、根据2Br-+Cl2═Br2+2Cl-可知氧化性是Cl2>Br2,符合题干已知条件,所以化学方程式成立,故B正确;
C、根据Br2+2I-═2Br-+I2可知氧化性是Br2>I2,符合题干已知条件,所以化学方程式成立,故C正确;
D、根据2Fe2++I2═2Fe3++2I-,可知氧化性是I2>Fe3+,不符合题干已知条件,所以化学方程式不成立,故D错误;
故选D.
点评 本题考查氧化还原反应,把握发生的反应及反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
相关题目
5.以下离子检验正确的是( )
| A. | 检验试液中的SO42-:试液$\stackrel{BaCl_{2}溶液}{→}$ 白色沉淀$\stackrel{HCl溶液}{→}$ 白色沉淀 | |
| B. | 检验试液中的Cl-:试液$\stackrel{稀H_{2}SO_{4}}{→}$无沉淀$\stackrel{AgNO_{3}溶液}{→}$ 白色沉淀 | |
| C. | 检验试液中的Fe2+:试液$\stackrel{氯水}{→}$无明显现象$\stackrel{KSCN溶液}{→}$血红色溶液 | |
| D. | 检验试液中的NH4+:试液$→_{供热}^{NaOH溶液}$气体逸出$→_{石蕊试纸}^{湿润的红色}$ 试纸变蓝 |
2.下列物质与CH3CH2OH互为同系物的是( )
| A. | H-OH | B. | CH3OH | C. |  | D. | CH3OCH3 |
9.糖类、油脂、蛋白质是人体维持生命活动的三大营养物质,下列说法正确的是( )
| A. | 葡萄糖、果糖、蔗糖和淀粉都能发生水解反应 | |
| B. | 利用油脂在碱性条件下的水解,可以制甘油和肥皂 | |
| C. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成的高分子化合物 | |
| D. | 淀粉和纤维素的分子组成相同,它们之间互为同分异构体 |
4.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,11.2L 氮气所含的原子数目为NA | |
| B. | 在反应3SiO2+6C+2N2=Si3N4+6CO,生成1 mol Si3N4时共转移12 NA电子 | |
| C. | 1molNa2O2固体中含离子总数为4 NA | |
| D. | 25℃时pH=13的NaOH溶液中含有Na+的数目为0.1NA |
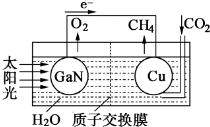 ,利用该装置成功地实现了以CO2和H2O合成CH4.写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O.为提高该人工光合系统的工作效率,可向装置中加入少量硫酸(填“盐酸”或“硫酸”).
,利用该装置成功地实现了以CO2和H2O合成CH4.写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O.为提高该人工光合系统的工作效率,可向装置中加入少量硫酸(填“盐酸”或“硫酸”).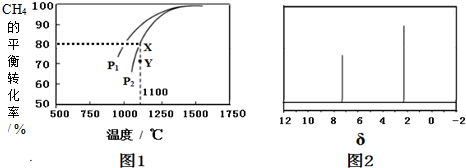
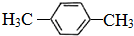 .(相对原子量:C-12 H-1)
.(相对原子量:C-12 H-1)