题目内容
18.若锌与稀硝酸反应时,其化学反应方程式为:4Zn+10HNO3=aZn(NO3)2+bM+cH2O,则a、b、c、M可能分别为( )| A. | 4、1、5、NO2 | B. | 4、2、4、NO2 | C. | 4、1、3、NH4NO3 | D. | 4、3、5、NO |
分析 由反应可知,Zn元素的化合价升高,则N元素的化合价降低,结合电子与原子守恒计算.
解答 解:由反应可知,Zn元素的化合价升高,则N元素的化合价降低,
①若M为NO2,由电子守恒可知,b=$\frac{4×(2-0)}{(5-4)}$=8,A、B错误;
②若M为NO,由电子守恒可知,b=$\frac{4×(2-0)}{(5-2)}$=$\frac{8}{3}$,D错误;
③若M为NH4NO3,由电子守恒可知,b=$\frac{4×(2-0)}{[5-(-3)]}$=1,结合原子守恒可知,a=4,c=3,
故选C.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与计算考查,注意电子守恒的应用,题目难度不大.

练习册系列答案
相关题目
1.一种气态烷烃与一种气态炔烃等体积混合,测得混合气体在标准状况下的密度为1.25g/L,则构成这种混合气体的烷烃和炔烃可能是( )
| A. | 甲烷,丙炔 | B. | 甲烷,丁炔 | C. | 乙烷,乙炔 | D. | 乙烷,丙炔 |
13.下列实验操作或鉴别方法可行的是( )
| A. | 蒸发操作时,应将混合物中的水分蒸干后,才能停止加热 | |
| B. | 用Ba(NO3)2溶液鉴别Cl-、SO42和CO32- | |
| C. | 用氨水鉴别Al3+、Mg2+和Ag+ | |
| D. | 可以用溶解过滤的方法从加热氯酸钾和二氧化锰的混合物中获得二氧化锰 |
7.下列推理正确的是( )
| A. | 铝粉在氧气中燃烧生成Al2O3,故钠在氧气中燃烧生成Na2O | |
| B. | 铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜 | |
| C. | 活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中 | |
| D. | 钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属单质均作还原剂 |
8.设NA表示阿伏伽德罗常数的值,下列说法中,正确的是( )
| A. | 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA | |
| B. | 1molAl3+含有核外电子数为3NA | |
| C. | 常温常压下,1mol氧气所含的原子数为NA | |
| D. | 1molNaCl晶体中含有NA个Na+和NA个Cl |
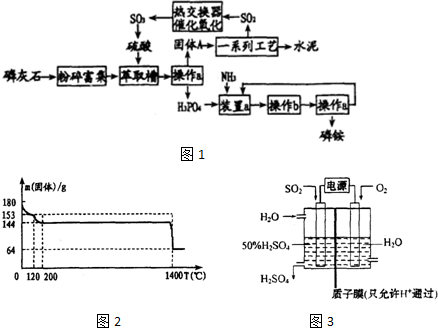
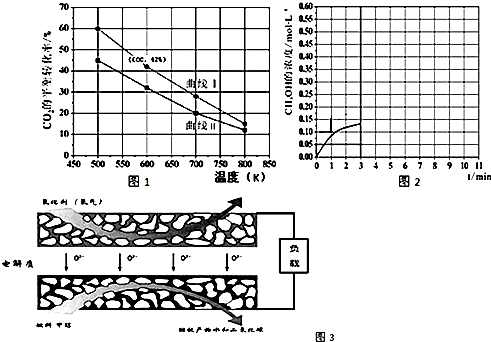
 甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题
甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题