题目内容
19.对以下描述的解释或结论中,正确的是( )| 选项 | 描述 | 解释或结论 |
| A | 向某溶液中加入BaCl2溶液生成白色沉淀,继续加稀硝酸沉淀不消失 | 溶液中含SO42- |
| B | Cl2+H2O=HClO+HCl | Cl2仅为还原剂,HCl为氧化产物 |
| C | PH=1的溶液中Fe2+、Al3+、SO42-、MnO4-不能大量共存 | 5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O |
| D | SO2使酸性高锰酸钾溶液和品红试液褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溶液中含有Ag+等离子会干扰SO42-的检验;
B.该反应中氯元素化合价由0价变为-1价和+1价,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂;
C.二价铁能被高锰酸根氧化;
D.二氧化硫与品红反应,使品红褪色,表现漂白性.
解答 解:A.溶液中含有Ag+等离子会干扰SO42-的检验,应先加入盐酸,没有白色沉淀生成,再加入氯化钡溶液,有白色沉淀产生,说明原溶液中含有SO42-,故A错误;
B.该反应中氯元素化合价由0价变为-1价和+1价,所以氯气既是氧化剂又是还原剂,HCl为还原产物,故B错误;
C.二价铁能被高锰酸根氧化,离子方程式:5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O,故C正确;
D.SO2具有还原性,可使酸性高锰酸钾溶液发生氧化还原反应而褪色,故D错误.
故选C.
点评 本题考查离子检验、氧化还原反应、二氧化硫的还原性、漂白性等,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意相关知识的积累,难度不大.

练习册系列答案
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
10.下列实验操作或实验事故处理正确的是( )
| A. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| B. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 实验时手指上不小心沾上苯酚,立即用70℃以上的热水清洗 | |
| D. | 苯中含苯酚杂质,除去杂质的方法:加入溴水,过滤 |
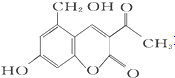
7.化合物M叫假蜜环菌素,它是香豆素类天然化合物.下列对M的叙述中错误( )
 M(假蜜环菌素)
M(假蜜环菌素)
 M(假蜜环菌素)
M(假蜜环菌素)| A. | M的分子式为C12H10O5 | |
| B. | 1 mol M最多可和6mol H2发生加成反应 | |
| C. | M可发生水解反应 | |
| D. | M可与 HBr反应 |
14.在A、B、C三支试管中分别加入等体积0.1 mol/L Fe2(SO4)3溶液.将A试管在酒精灯火焰上加热到沸腾,向B试管中加3滴6 mol/L H2SO4.下列说法不正确的是( )
| A. | 最终三支试管的颜色各不相同 | |
| B. | A试管中Fe(OH)3含量最高 | |
| C. | 直接加热蒸发Fe2(SO4)3溶液可得到Fe2(SO4)3晶体 | |
| D. | B试管中Fe2(SO4)3不能发生水解 |
4.依据下列实验现象,得出的结论正确的是( )
| 操作 | 实验现象 | 结论 | |
| A | 向NaBr溶液中加入氯水,再加入淀粉KI溶液 | 溶液变蓝 | 氧化性:Cl2>Br2>I2 |
| B | 将铝片放入盐酸中 | 产生气泡的速率开始较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
| C | 向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性 |
| D | 向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 | 品红溶液褪色 | 气体中含有Cl2 |
| A. | A | B. | B | C. | C | D. | D |
4.化学与人类生活、生成和社会可持续发展密切相关,下列说法正确的是( )
| A. | 铜矿石在细菌作用下直接转换为单质铜,这个过程中叫做生物炼铜 | |
| B. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,相同条件下,某物质的热值越高,其标准燃烧越大 | |
| C. | 铅蓄电池是最常见的二次电池,可根据硫酸的密度来判断铅蓄电池是否需要充电 | |
| D. | “地沟油”禁止食用,但可以通过物理变化制肥皂 |
1.室温时,浓度均为0.1mol•L-1的三种酸HX、HY、HZ,稀释时的pH变化如图所示.下列判断正确的是( )


| A. | 等体积的三种酸与足量Mg反应,HX放出气体的体积最小 | |
| B. | 三种酸等体积混合后与NaOH溶液反应,当HX恰好完全反应时:c(Y-)>c(X-)>c(OH-)>c(H+) | |
| C. | 根据曲线,可得0.1mol•L-1HX溶液中由水电离出的c(H+)为10-4mol•L-1 | |
| D. | 将HY与HZ的稀溶液混合后所得溶液中:c(H+)=$\frac{{K}_{a}(HY)•c(HY)}{c({H}^{+})}$+c(Z-)+c(OH-) |
2.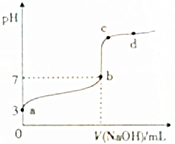 常温下,向20mL0.1mol•L-1CH3COOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
常温下,向20mL0.1mol•L-1CH3COOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
 常温下,向20mL0.1mol•L-1CH3COOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
常温下,向20mL0.1mol•L-1CH3COOH溶液中逐滴加入0.1mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )| A. | a点表示的溶液中:c(H+)>c(CH3COO-)>c(OH-) | |
| B. | b点时,V(NaOH)=20mL | |
| C. | c点表示的溶液中:c(H+)+c(Na+)=c(OH-)+c(CH3COO-) | |
| D. | d点表示的溶液中:c(Na+)>c(CH3COO-) |