��Ŀ����
1������ʱ��Ũ�Ⱦ�Ϊ0.1mol•L-1��������HX��HY��HZ��ϡ��ʱ��pH�仯��ͼ��ʾ�������ж���ȷ���ǣ�������
| A�� | �������������������Mg��Ӧ��HX�ų�����������С | |
| B�� | ������������Ϻ���NaOH��Һ��Ӧ����HXǡ����ȫ��Ӧʱ��c��Y-����c��X-����c��OH-����c��H+�� | |
| C�� | �������ߣ��ɵ�0.1mol•L-1HX��Һ����ˮ�������c��H+��Ϊ10-4mol•L-1 | |
| D�� | ��HY��HZ��ϡ��Һ��Ϻ�������Һ�У�c��H+��=$\frac{{K}_{a}��HY��•c��HY��}{c��{H}^{+}��}$+c��Z-��+c��OH-�� |
���� 0.1000mol•L-1��������HX��HY��HZ��pH�ֱ�Ϊ4��3��1�������Դ�СΪHX��HY��HZ��0.1mol•L-1��HZ��pH=1��˵��HZΪǿ�ᣬHX��HYΪ���ᣬ�Դ˽����⣮
��� �⣺0.1000mol•L-1��������HX��HY��HZ��pH�ֱ�Ϊ4��3��1�������Դ�СΪHX��HY��HZ��
A����ΪһԪ�ᣬ������������������ʵ�����ȣ����������������ȣ���A����
B��HXǡ����ȫ��Ӧʱ��HY���Ѿ���ȫ��Ӧ��������ҺΪNaX��NaY���Һ������ HX��HY��NaYˮ��̶�С��NaX������Һ��c��X-����c��Y-����c��Y-����c��X-����c��OH-����c��H+������B��ȷ��
C���������ߣ��ɵ�0.1mol•L-1HX��ҺpH=4������ˮ�������c��H+��Ϊ10-10mol•L-1����C����
D��HY��HZ��ϣ���Һ�е���غ�Ϊc��H+��=c��Y-��+c��Z-��+c��OH-�����ٸ���HY�ĵ���ƽ�ⳣ����c��Y-��=$\frac{{K}_{a}��HY��•c��HY��}{c��{H}^{+}��}$����c��H+��=$\frac{{K}_{a}��HY��•c��HY��}{c��{H}^{+}��}$+c��Z-��+c��OH-������D��ȷ��
��ѡBD��
���� ���⿼������Һ���������ҺpH�ļ��㡢����ϵĶ����жϡ���Һ������Ũ�ȴ�С�Ƚϣ���Ŀ�Ѷ��еȣ�ע����������ϵĶ����жϼ��й���ҺpH�ļ��㷽������ȷ����������ͼ����ϢΪ�����Ĺؼ����ܹ����ݵ���غ㡢�����غ㡢�ε�ˮ��ԭ���Ƚ���Һ�и�����Ũ�ȴ�С��

 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�| A�� | һ��С�ڵ��ʾһ������ | B�� | �ڵ�Ķ��ٱ�ʾ���Ӹ����Ķ��� | ||
| C�� | ��ʾ�����˶��Ĺ켣 | D�� | �����ں���ռ���ֻ���Ķ��� |
| ѡ�� | ���� | ���ͻ���� |
| A | ��ij��Һ�м���BaCl2��Һ���ɰ�ɫ������������ϡ�����������ʧ | ��Һ�к�SO42- |
| B | Cl2+H2O=HClO+HCl | Cl2��Ϊ��ԭ����HClΪ�������� |
| C | PH=1����Һ��Fe2+��Al3+��SO42-��MnO4-���ܴ������� | 5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O |
| D | SO2ʹ���Ը��������Һ��Ʒ����Һ��ɫ | SO2����Ư���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | O.1molNa2O2��ˮ��Ӧת�Ƶ�����ĿΪ0.1NA | |
| B�� | ����£�2.24LCl2���µ��ӶԵ���ĿΪ0.2NA | |
| C�� | PH=2��H2SO4��Һ�к�H+����ĿΪ0.12NA | |
| D�� | ��10g��������Ϊ17%�İ�ˮ�У�����H����ĿΪ0.3NA |

| A�� | t1ʱ��ֻ��������Ӧ | B�� | t1��t2��X2�����ʵ���Խ��Խ�� | ||
| C�� | t2��t3����Ӧ���ٷ��� | D�� | t2��t3�������ʵ�Ũ�Ȳ��ٷ����仯 |

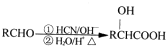
 ��
�� ��
�� Ŀǰ��ȫ��������������������ͭ������Ǧ��п������ɫ��������λ������ҵ��չ�̲��ž�DZ����
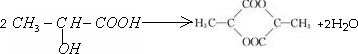
Ŀǰ��ȫ��������������������ͭ������Ǧ��п������ɫ��������λ������ҵ��չ�̲��ž�DZ���� ����HCHO�ȣ����з�������ƽ��ṹ���Т٢ڢۢܣ���������ţ���Ԥ��HCHO���ӵ�����ṹΪƽ�������Σ�
����HCHO�ȣ����з�������ƽ��ṹ���Т٢ڢۢܣ���������ţ���Ԥ��HCHO���ӵ�����ṹΪƽ�������Σ� ������������һ����ԭ�ӣ�������ԭ�Ӷ��ھ������ϣ���ԭ�Ӷ��ھ��������ϣ��þ���Ļ�ѧʽΪNi5La��LaNi5��
������������һ����ԭ�ӣ�������ԭ�Ӷ��ھ������ϣ���ԭ�Ӷ��ھ��������ϣ��þ���Ļ�ѧʽΪNi5La��LaNi5�� ��1��Cu2+����NH3��Cl-���γ���λ��Ϊ4��������֪[Cu��NH3��4]2+���жԳƵĿռ乹�ͣ�[Cu��NH3��4]2+�е�����NH3������Cl-ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ����[Cu��NH3��4]2+�Ŀռ乹��Ϊƽ�������Σ�
��1��Cu2+����NH3��Cl-���γ���λ��Ϊ4��������֪[Cu��NH3��4]2+���жԳƵĿռ乹�ͣ�[Cu��NH3��4]2+�е�����NH3������Cl-ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ����[Cu��NH3��4]2+�Ŀռ乹��Ϊƽ�������Σ�
 ��C
��C ��
�� ��
�� ��
�� ��
��