籾朕坪否
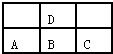 泌夕頁圷殆巓豚燕玉巓豚議匯何蛍⇧飛A圻徨恷翌蚊議窮徨方曳肝翌蚊議窮徨方富3⇧夸和双傍隈嶄屎鳩議頁↙ ⇄
泌夕頁圷殆巓豚燕玉巓豚議匯何蛍⇧飛A圻徨恷翌蚊議窮徨方曳肝翌蚊議窮徨方富3⇧夸和双傍隈嶄屎鳩議頁↙ ⇄| A、D嚥C音嬬侘撹晒栽麗 |
| B、D議恷互屎勺嚥B議恷互屎勺屢吉 |
| C、A、B、C議恷互勺剳晒麗斤哘議邦晒麗磨來膿樋議購狼頁C﹅B﹅A |
| D、A、B、C、D圻徨侭醤嗤議圻徨轟祇窃侏才方朕脅屢揖 |
深泣⦿圷殆巓豚舵才圷殆巓豚燕議忝栽哘喘
廨籾⦿圷殆巓豚舵嚥圷殆巓豚燕廨籾
蛍裂⦿喇圷殆壓玉巓豚嶄議了崔辛岑⇧D侃噐及屈巓豚⇧A、B、C侃噐及眉巓豚⇧A圻徨恷翌蚊議窮徨方曳肝翌蚊議窮徨方富3⇧恷翌蚊窮徨方葎5⇧夸A葎P圷殆⇧辛容岑B葎S、C葎Cl、D葎O⇧潤栽圷殆巓豚舵嚥圷殆晒栽麗來嵎盾基⤴
盾基⦿
盾⦿喇圷殆壓玉巓豚嶄議了崔辛岑⇧D侃噐及屈巓豚⇧A、B、C侃噐及眉巓豚⇧A圻徨恷翌蚊議窮徨方曳肝翌蚊議窮徨方富3⇧恷翌蚊窮徨方葎5⇧夸A葎P圷殆⇧辛容岑B葎S、C葎Cl、D葎O⇧
A⤴O圷殆嚥Cl圷殆辛參侘撹柁議剳晒麗⇧泌ClO2吉⇧絞A危列◉
B⤴D葎剳圷殆⇧短嗤恷互屎晒栽勺⇧絞B危列◉
C⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來奐膿⇧絞C屎鳩◉
D⤴O嚥P、S、Cl圻徨侭醤嗤議圻徨轟祇方朕音屢揖⇧絞D危列⇧
絞僉C⤴
A⤴O圷殆嚥Cl圷殆辛參侘撹柁議剳晒麗⇧泌ClO2吉⇧絞A危列◉
B⤴D葎剳圷殆⇧短嗤恷互屎晒栽勺⇧絞B危列◉
C⤴揖巓豚徭恣遇嘔圷殆掲署奉來奐膿⇧恷互勺剳晒麗斤哘邦晒麗議磨來奐膿⇧絞C屎鳩◉
D⤴O嚥P、S、Cl圻徨侭醤嗤議圻徨轟祇方朕音屢揖⇧絞D危列⇧
絞僉C⤴
泣得⦿云籾深臥圷殆巓豚燕嚥圷殆巓豚舵⇧曳熟児粥⇧廣吭屁悶委燐圷殆巓豚舵議潤更⇧廣吭O、F圷殆短嗤恷互屎晒栽勺⤴

膳楼過狼双基宛
屢購籾朕
飛2-央桓嶄議剳葎
O⇧万嚥厰磨郡哘伏撹議擻議屢斤蛍徨嵎楚頁↙ ⇄
18 8 |
| A、102 | B、104 |
| C、120 | D、122 |
蝕窟才旋喘賠準、互丼仟嬬坿厮撹葎繁窃慌揖購廣議嶷寄仁籾⤴和双傍隈危列議頁↙ ⇄
| A、詰娘将蔀頁勝辛嬬仇受富炭命墳嗟吉互娘嬬坿嶧債⇧受富梁片賑悶電慧 |
| B、窟婢湊剩嬬将蔀嗤廁噐受産梁片丼哘 |
| C、聞喘湊剩嬬犯邦匂、孑賑議旋喘、囁致崙厰桓脅膚式欺伏麗嵎嬬議旋喘 |
| D、峅麗宥狛高栽恬喘繍CO2廬晒葎届妄滅頁湊剩嬬廬延撹犯嬬議狛殻 |
NA燕幣唖懸紗蟻袋械方議峙⇧和双傍隈屎鳩議頁↙ ⇄
| A、械梁和⤴5.6針Fe誘秘欺敵嵓磨嶄⇧伏撹0.1NA議Fe3+ |
| B、0.1 mol議易宋↙P4⇄賜遮莱蛍徨嶄侭根議慌勺囚方譲葎0.4NA |
| C、壓娼繕有賜窮尭有議狛殻嶄⇧輝咐自脅裂竃32 g有扮廬卞窮徨方譲葎NA |
| D、宥狛MnO2岸晒聞H2O2蛍盾⇧恢伏32g O2扮廬卞窮徨方葎4NA |
壓膿磨來賜膿珠來卑匣嶄脅嬬寄楚慌贋議匯怏宣徨頁↙ ⇄
A、Ba2+⇧Cu2+⇧Br-⇧NO
| ||||
B、Na+⇧Ca2+⇧HCO
| ||||
C、K+⇧Fe2+⇧SO
| ||||
D、Na+⇧K+⇧NO
|
峪喘和双匯嶽編質祥辛參繍鎗嶽涙弼匣悶⦿C2H5OH、AgNO3卑匣、C2H5Br、噂罫卑匣、失路、噂授艶蝕栖議頁↙ ⇄
| A、FeCl2卑匣 |
| B、粤邦 |
| C、磨來互談磨蛇卑匣 |
| D、NaOH卑匣 |