题目内容
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、常温下.5.6克Fe投入到浓硝酸中,生成0.1NA的Fe3+ |
| B、0.1 mol的白磷(P4)或甲烷分子中所含的共价键数均为0.4NA |
| C、在精炼铜或电镀铜的过程中,当阴极都析出32 g铜时转移电子数均为NA |
| D、通过MnO2催化使H2O2分解,产生32g O2时转移电子数为4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.常温下,铁与浓硝酸发生钝化,阻止了反应的继续进行;
B.白磷分子为四面体结构,分子中存在6个P-P共价键;
C.根据电子守恒判断,32g铜的物质的量为0.5mol,生成0.5mol铜需要转移1mol电子;
D.双氧水中氧元素化合价为-1价,根据氧气的物质的量计算出转移的电子数.
B.白磷分子为四面体结构,分子中存在6个P-P共价键;
C.根据电子守恒判断,32g铜的物质的量为0.5mol,生成0.5mol铜需要转移1mol电子;
D.双氧水中氧元素化合价为-1价,根据氧气的物质的量计算出转移的电子数.
解答:
解:A.常温下,铁遇到浓硝酸发生钝化,无法计算转移的电子数,故A错误;
B.0.1mol白磷分子中含有0.6mol共价键,0.1mol甲烷中含有0.4mol碳氢共价键,二者含有的共价键数目不同,故B错误;
C.32g铜的物质的量为0.5mol,电解过程中阴极只有铜离子放电,生成0.5mol铜需要转移1mol电子,转移电子数均为NA,故C正确;
D.32g氧气的物质的量为1mol,双氧水中氧元素化合价由-1价变成氧气的0价,生成1mol氧气转移2mol电子,转移电子数为2NA,故D错误;
故选C.
B.0.1mol白磷分子中含有0.6mol共价键,0.1mol甲烷中含有0.4mol碳氢共价键,二者含有的共价键数目不同,故B错误;
C.32g铜的物质的量为0.5mol,电解过程中阴极只有铜离子放电,生成0.5mol铜需要转移1mol电子,转移电子数均为NA,故C正确;
D.32g氧气的物质的量为1mol,双氧水中氧元素化合价由-1价变成氧气的0价,生成1mol氧气转移2mol电子,转移电子数为2NA,故D错误;
故选C.
点评:本题考查了阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项A为易错点,注意常温下铁、铝与浓硫酸、浓硝酸发生钝化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
X、Y、Z、W为四种短周期主族元素.其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法不正确的是( )
| A、Y元素最高价氧化物对应水化物的化学式为HY04 |
| B、原子半径由小到大的顺序为W<X<Z |
| C、X与W可以形成W2X、W2X2两种物质 |
| D、Y、Z两元素的气态氢化物中,Z的气态氢化物更稳定 |
下列物质中,能在X射线透视肠胃时用作“钡餐”的是( )
| A、BaSO4 |
| B、BaCO3 |
| C、BaCl2 |
| D、NaCl |
下列离子方程式正确的是( )
| A、氢氧化钡与稀硫酸混合:SO42-+H++OH-+Ba2+=H2O+BaSO4↓ |
| B、碳酸氢钠溶液与NaOH溶液混合:HCO3-+OH-=H2O+CO32- |
| C、石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
| D、氧化铜与盐酸反应 O2-+2H+=H2O |
含相同分子数的CO2和NH3一定具有相同的( )
| A、原子个数 | B、体积 |
| C、质量 | D、物质的量 |
下列不属于毒品,但能增加兴奋度的是( )
| A、吗啡 | B、海洛因 |
| C、冰毒 | D、麻黄碱 |
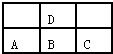 如图是元素周期表短周期的一部分,若A原子最外层的电子数比次外层的电子数少3,则下列说法中正确的是( )
如图是元素周期表短周期的一部分,若A原子最外层的电子数比次外层的电子数少3,则下列说法中正确的是( )| A、D与C不能形成化合物 |
| B、D的最高正价与B的最高正价相等 |
| C、A、B、C的最高价氧化物对应的水化物酸性强弱的关系是C>B>A |
| D、A、B、C、D原子所具有的原子轨道类型和数目都相同 |
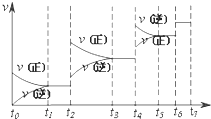 在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据:
在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据: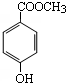 分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质在食品、化妆品等行业有广泛用途.
分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质在食品、化妆品等行业有广泛用途.