题目内容
20.根据乙烯和乙醇的知识填空.(1)完成下列化学方程式:CH2=CH2+HCl→CH3CH2Cl;
(2)实验室,乙醇跟钠发生反应,产生的气体是H2.
分析 (1)乙烯含有碳碳双键,能够发生加成反应,依据加成反应特点结合原子个数守恒判断;
(2)乙醇与钠反应生成乙醇钠和氢气.
解答 解:(1)乙烯含有碳碳双键,能够发生加成反应,依据方程式所结合反应物与生成物结合原子个数守恒可知,二者反应方程式:CH2=CH2+HCl→CH3CH2Cl;
故答案为:HCl;
(2)乙醇与钠反应生成乙醇钠和氢气,方程式:2Na+2CH3CH2OH=2CH3CH2ONa+H2↑,所以生成气体为氢气,化学式为:H2;
故答案为:H2.
点评 本题考查了化学方程式的书写,侧重考查有机反应方程式,明确乙烯、乙醇的结构及性质是解题关键,题目难度不大.

练习册系列答案
相关题目
8.将ag Na放入水中,完全反应后要使所得溶液中每b个水分子中溶有1个Na+,需水的量为( )
| A. | $\frac{ab}{23}$mol | B. | $\frac{a(b+1)}{23}$mol | C. | $\frac{18ab}{23}$g | D. | $\frac{18a(b+1)}{23}$mol |
12.某混合物,可能含有以下几种离子:K+、Cl-、NH4+、Mg2+、CO32-、Ba2+、SO42-,若将该混合物溶于水可得澄清溶液,现取3份各100mL该溶液分别进行如下实验:
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是不能确定(填“一定存在”“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是Ba2+、Mg2+.
(2)试确定溶液中一定存在的阴离子及其物质的量浓度((可以不填满,也可以增加)):
(3)试确定K+是否存在?存在,如果存在,c(K+)溶液中肯定存在的离子是NH4+、CO32-和SO42-,经计算,NH4+的物质的量为0.05 mol,CO32-、SO42-的物质的量分别为0.01 mol和0.02 mol,根据电荷守恒得K+一定存在,且钾离子的物质的量浓度为:≥0.1mol/l,如果不存在,理由是、.
| 实验 序号 | 实验内容 | 实验结果 |
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
| 3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.63g,第二次称量读数为4.66g |
(1)根据实验1对Cl-是否存在的判断是不能确定(填“一定存在”“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是Ba2+、Mg2+.
(2)试确定溶液中一定存在的阴离子及其物质的量浓度((可以不填满,也可以增加)):
| 阴离子符号 | 物质的量浓度(mol/L) |
9.下列反应能说明苯环对侧链有影响的是( )
| A. | 对二甲苯与酸性高锰酸钾溶液发生反应;甲烷与酸性高锰酸钾溶液不反应 | |
| B. | 甲苯与浓硝酸和浓硫酸混合液,加热;苯与浓硝酸和浓硫酸混合液,加热 | |
| C. | 乙苯与氢气在催化剂作用下加热反应;苯与氢气在催化剂作用下加热反应 | |
| D. | 邻二甲苯与氯气在光照下发生反应;甲烷在光照下与氯气发生反应 |
10.下列各组物质的溶液,分别只用一种试剂一次就可加以区别的是( )
| A. | Na2SO4、BaC12、K2CO3、KNO3 | B. | HC1、NaNO3、Na2CO3、(NH4)2SO4 | ||
| C. | NaOH、KC1、K2CO3、MgCl2 | D. | NaAlO2、NaC1、Na2CO3、AgNO3 |
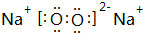 .
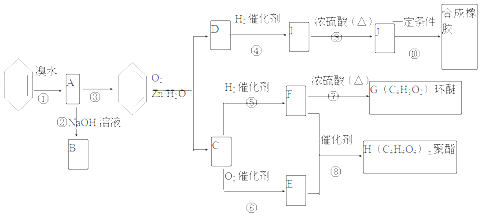
.
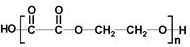
 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$ +2NaBr.C与足量银氨溶液反应的化学方程式OHC-CHO+4[Ag(NH3)2]OH
+2NaBr.C与足量银氨溶液反应的化学方程式OHC-CHO+4[Ag(NH3)2]OH H4NOOCCOONH4+4Ag↓+6NH3+2H2O
H4NOOCCOONH4+4Ag↓+6NH3+2H2O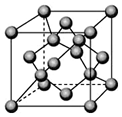 已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子.B的基态原子核外电子有9种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答:
已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子.B的基态原子核外电子有9种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答: