题目内容
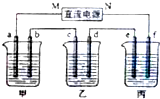 如图所示装置中,甲、乙、丙三个烧杯依次盛有NaOH溶液、CuSO4溶液和Na2SO4溶液,电极均为石墨电极,接通电源,经过一段时间后,测得乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次盛有NaOH溶液、CuSO4溶液和Na2SO4溶液,电极均为石墨电极,接通电源,经过一段时间后,测得乙中c电极质量增加.据此回答问题:(1)电极b上发生的电极反应为
(2)电解前后丙溶液的酸碱性大小是否发生变化,简述其原因
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)乙中C电极质量增加,则c处发生的反应为:Cu2++2e-=Cu,即C处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极;
(2)丙中为电解水,对于Na2SO4而言,其pH几乎不变.
(2)丙中为电解水,对于Na2SO4而言,其pH几乎不变.
解答:
解:(1)乙中C电极质量增加,则c处发生的反应为:Cu2++2e-=Cu,即C处为阴极,由此可推出b为阳极,甲中为NaOH,相当于电解H2O,阳极b处为阴离子OH-放电,即4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑;
(2)丙中电解质为Na2SO4,Na2SO4是强酸强碱正盐,溶液显中性,电解时在阳极氢氧根离子放电,在阴极氢离子放电,用石墨电极电解Na2SO4溶液实质是电解水,
其pH不变,故答案为:酸碱性大小没有变化,因为Na2SO4是强酸强碱正盐,用石墨电极电解Na2SO4溶液实质是电解水.
(2)丙中电解质为Na2SO4,Na2SO4是强酸强碱正盐,溶液显中性,电解时在阳极氢氧根离子放电,在阴极氢离子放电,用石墨电极电解Na2SO4溶液实质是电解水,
其pH不变,故答案为:酸碱性大小没有变化,因为Na2SO4是强酸强碱正盐,用石墨电极电解Na2SO4溶液实质是电解水.
点评:本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,准确判断两极上离子的放电顺序.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
稀氨水中存在下述平衡:NH3+H20?NH3?H2O?NH4++OH-改变下列条件,能使电离程度增大的是( )
| A、加浓氨水 |
| B、升高温度 |
| C、加NH4Cl溶液 |
| D、加NaOH溶液 |
在一定条件下发生下列反应,其中属于盐类水解反应的是( )
| A、HS-+H+═H2S |
| B、HCO3-+H2O?H3O++CO32- |
| C、NH4++H2O?NH3?H2O+H+ |
| D、Cl2+H2O?H++Cl-+HClO |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2 |
| B、碱性氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- |
| C、NH4Cl溶液显酸性的原因:NH4++H2O?NH3↑+H2O+H+ |
| D、Na2CO3的水解离子方程式:CO32-+2H2O?H2CO3+2OH- |
下列有关人体发胖的说法不科学的是( )
| A、人体发胖是脂肪在人体中的积累 |
| B、葡萄糖在酶催化下经过一系列反应也能在体内转化为脂肪 |
| C、胖子们说自己光喝水也会发胖 |
| D、过量食用酸性食物易引起发胖 |
诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是( )
| A、纤维素,脂肪 |
| B、蛋白质,高级烃 |
| C、淀粉,油脂 |
| D、蛋白质,硬化油 |
25℃时,用0.01mol?L-1H2SO4溶液滴定0.01mol?L-1NaOH溶液,中和后加水至100mL.若在滴定时终点判断有误差:①多加了1滴H2SO4溶液;②少加了1滴H2SO4溶液(设1滴为0.05mL),则①和②的溶液中由水电离出的c(H+)之比的值是( )
| A、1 |
| B、50 |
| C、2.5×103 |
| D、104 |
下列离子方程式书写正确的是( )
| A、钠和水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| B、FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| C、铜和浓HNO3反应:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O |
| D、NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |