题目内容
5.如图为农夫山泉矿泉水瓶上的部分说明文字,列出了饮用天然水理化指标,这里的钙、钾、钠是指( )
| A. | 原子 | B. | 分子 | C. | 单质 | D. | 元素 |
分析 矿泉水瓶上的钙、钾、钠指元素的含量,原子和分子都是微观粒子,难测定,农夫山泉中不存在金属单质,则不会是单质的含量,据此进行判断.
解答 解:A.原子为微观粒子,很难进行测定,故A错误;
B.分子是微观粒子,很难进行测定,故B错误;
C.钙、钾、钠是活泼金属,能和水反应生成其它物质,所以水中不可能含有这几种单质,故C错误;
D.农夫山泉含有钙、钾、钠元素,故D正确;
故选D.
点评 本题考查了元素与原子、分子及单质的关系,题目难度不大,注意熟悉生活中常见饮料中的含量是指测定元素的含量,明确元素与分子、原子等之间关系.

练习册系列答案
相关题目
16.下列物质分类正确的是( )
| A. | SO2、SiO2、CO2均为酸性氧化物 | |
| B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| C. | 烧碱、冰醋酸、四氯化碳、氨气均为电解质 | |
| D. | 福尔马林、水玻璃、氢氟酸、小苏打均为纯净物 |
17.已知氮的氧化物具有氧化性,能与灼热的铜反应生成氧化铜和氮气.将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为( )
| A. | N2O3 | B. | NO2 | C. | N2O | D. | N2O4 |
15.下列说法或表达正确的是( )
| A. | H2SO4的摩尔质量是98 | |
| B. | 通电时,溶液中的溶质分子分别向两极移动,胶体中的分散质粒子向某一极移动 | |
| C. | 丁达尔效应可用于区别溶液和胶体,云、雾均能产生丁达尔效应 | |
| D. | 将98gH2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2mol/L |
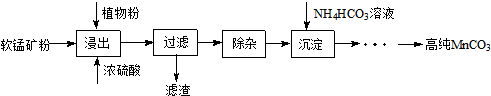
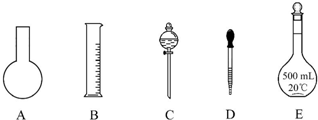
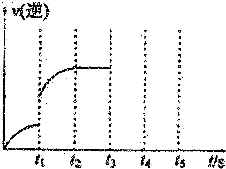 Ⅰ.体积为5L的恒温、恒容密闭容器甲起始投入2molN2、3molH2经过l0s达平衡,测得平衡时NH3的物质的量为0.8mol.
Ⅰ.体积为5L的恒温、恒容密闭容器甲起始投入2molN2、3molH2经过l0s达平衡,测得平衡时NH3的物质的量为0.8mol. 营养品和药品都是保证人类健康不可缺少的物质,其性质和制法是化学研究的主要内容.已知酪氨酸是一种生命活动不可缺少的氨基酸,它的结构简式是:
营养品和药品都是保证人类健康不可缺少的物质,其性质和制法是化学研究的主要内容.已知酪氨酸是一种生命活动不可缺少的氨基酸,它的结构简式是: .
.