题目内容
下面说法正确的是( )
| A、摩尔是七个基本物理量之一 |
| B、摩尔是物质的量的单位 |
| C、物质的量就是物质的质量 |
| D、阿伏加德罗常数就是6.02×1023 |
考点:物质的量的单位--摩尔,阿伏加德罗常数
专题:化学用语专题
分析:A.摩尔是单位;
B.物质的量的单位是摩尔;
C.物质的量是一个物理量而非“物质的质量”,它表示含有一定数目粒子的集合体;
D.阿伏加德罗常数为6.02×1023mol-1.
B.物质的量的单位是摩尔;
C.物质的量是一个物理量而非“物质的质量”,它表示含有一定数目粒子的集合体;
D.阿伏加德罗常数为6.02×1023mol-1.
解答:
解:A.摩尔是七个基本物理量中物质的量的单位,故A错误;
B.摩尔是七个基本物理量中物质的量的单位,故B正确;
C.物质的量与质量是两个不同的物理量,故C错误;
D.阿伏加德罗常数为6.02×1023mol-1,有单位,故D错误.
故选B.
B.摩尔是七个基本物理量中物质的量的单位,故B正确;
C.物质的量与质量是两个不同的物理量,故C错误;
D.阿伏加德罗常数为6.02×1023mol-1,有单位,故D错误.
故选B.
点评:本题考查物质的量,难度不大,掌握物质的量的含义、单位、应用等是正确解答本题的关键.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
将0.51mol铜与250mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.待产生的气体全部释放后,向溶液中加入300mL5mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀.则下列选项正确的是( )
| A、产生NO气体0.24mol |
| B、产生NO2气体0.26mol |
| C、原HNO3浓度为8mol/L |
| D、原HNO3浓度为2mol/L |
以下分类正确的是( )
| 单质 | 混合物 | 电解质 | |
| A | 铜 | 冰水 | 氯化氢 |
| B | 水银 | 空气 | 氯化银 |
| C | 石墨 | 碘酒 | 二氧化碳 |
| D | 液氯 | 漂白粉 | 食盐水 |
| A、A | B、B | C、C | D、D |
下列实验操作中错误的是( )
| A、蒸发操作时,应残留少许液体,停止加热,再利用余热使水分完全蒸干 |
| B、由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、蒸馏操作时,应使温度计水银球上端与蒸馏烧瓶的支管口下端相平 |
下列有关物质的性质及该性质的应用表述均正确的是( )
| A、次氯酸钠具有强氧化性,可用于配制消毒液 |
| B、氨气具有还原性,可用作制冷剂 |
| C、氢氧化铁胶体具有吸附性,可用于除去水中所有杂质 |
| D、浓硫酸具有脱水性,可用作干燥剂 |
相同条件下,下列装置中指定电极的电极反应式相同的是( )
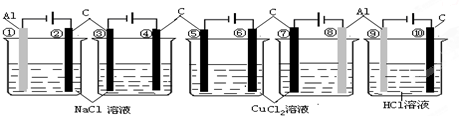

| A、②④⑥⑦⑩ |
| B、①③⑤⑧⑨ |
| C、②③④⑤⑥⑦⑩ |
| D、①③⑤⑦⑨ |
对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),叙述正确的( )
| A、单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达平衡状态 |
| B、达到化学平衡时,4v正(O2)=5v逆(NO) |
| C、化学反应速率关系是:3正(NH3)=2v正(H2O) |
| D、达到平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |

