题目内容
7.下列分离方法不正确的是( )| A. | 用过滤法除去Na2SO4溶液中的泥沙 | B. | 用蒸馏法分离溶液中的KCl和KNO3 | ||
| C. | 用萃取法将碘水中的I2萃取出来 | D. | 用蒸发法从NaCl溶液中得到NaCl |
分析 A.泥沙不溶于水,Na2SO4溶于水;
B.KCl、KNO3的溶解度受温度影响不同;
C.碘不易溶于水,易溶于有机溶剂;
D.NaCl能溶于水.
解答 解:A.泥沙不溶于水,则用过滤法除去Na2SO4溶液中的泥沙,故A正确;
B.KCl、KNO3的溶解度受温度影响不同,则选择结晶法分离,故B错误;
C.碘不易溶于水,易溶于有机溶剂,则用萃取法将碘水中的I2萃取出来,故C正确;
D.NaCl能溶于水,则用蒸发法从NaCl溶液中得到NaCl,故D正确;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
18.“美丽中国”是十八大提出的重大课题,她突出了生态文明,重点是社会发展与自然环境之间的和谐,下列针对这一主题的说法中错误的是( )
| A. | 推广燃煤脱硫技术,减少SO2污染,同时把煤粉碎了再燃烧以提高煤的燃烧效率 | |
| B. | 开发太阳能、风能和氢能等能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| D. | 在汽车尾气处理器中使用新的催化剂,促使平衡2CO+2NO?2CO2+N2向正反应方向移动,减少污染物的排放 |
15.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol羟基中含有的电子数为0.9 NA | |
| B. | 标准状况下,12g金刚石中含共价键的数目为4NA | |
| C. | 0.1 mol N2与足量H2充分反应,转移的电子数为0.6 NA | |
| D. | 235g核素92235U发生裂变反应:92235U+01n$\stackrel{裂变}{→}$2890Sr+54136Xe+1001n净产生的中子(01n)数为10NA |
2.两种气态的烃组成的混合物0.1mol完全燃烧可生成3.584L(标况)二氧化碳和3.6g水,则混合物中( )
| A. | 可能含有丙炔 | B. | 一定没有乙烷 | C. | 一定含有甲烷 | D. | 可能有乙烯 |
12.往20mL、0.1mol/L醋酸中滴加0.1mol/LNaOH溶液到溶液呈中性时,下列符合情况的是( )
| A. | 消耗NaOH溶液20mL | |
| B. | 溶液的PH值一定恰好等于7 | |
| C. | 溶液中只有醋酸钠 | |
| D. | 反应后溶液中醋酸根离子的浓度与钠离子溶液相等 |
19.下列关于接触法制硫酸的叙述,不正确的是( )
| A. | 黄铁矿的主要成分是FeS | B. | SO3与水反应是放热反应 | ||
| C. | 用98.3%的硫酸吸收SO3 | D. | 热交换的目的是充分利用反应热 |
5.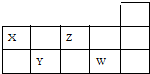 短周期X、Y、Z、W四种元素在元素周期表中位置如图所示.有关表述正确的是( )
短周期X、Y、Z、W四种元素在元素周期表中位置如图所示.有关表述正确的是( )
 短周期X、Y、Z、W四种元素在元素周期表中位置如图所示.有关表述正确的是( )
短周期X、Y、Z、W四种元素在元素周期表中位置如图所示.有关表述正确的是( )| A. | X、Y、W的最高价氧化物对应水化物均属强酸 | |
| B. | Y的氢化物能与Y的最高价氧化物对应水化物反应 | |
| C. | 原子半径从大到小依次为Y>W>X>Z | |
| D. | Z的氢化物的沸点低于W的氢化物 |
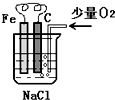 分析图,按要求写出有关反应方程式:
分析图,按要求写出有关反应方程式: