题目内容
16.为测定某样品中所含晶体FeSO4•7H2O的质量分数,取晶体样品a g,溶于稀硫酸配成100.00mL溶液,取出20.00mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应).若消耗0.2000mol•L-1 KMnO4溶液20.00mL,所得晶体中FeSO4•7H2O的质量分数为$\frac{13.9}{a}$(用a表示).分析 根据元素守恒和电子守恒,即5FeSO4•7H2O~KMnO4,计算FeSO4•7H2O的质量分数,由此分析解答.
解答 解:亚铁离子会被高锰酸钾氧化为三价铁离子,KMnO4被还原为+2价的锰离子,根据电子守恒,即5FeSO4•7H2O~KMnO4,根据消耗0.1000mol•L-1 KMnO4溶液20.00mL,所以晶体中FeSO4•7H2O的质量分数=$\frac{0.1000mol/L×0.02L×5×278g/mol}{ag}$×100%=$\frac{13.9}{a}$,
故答案为:$\frac{13.9}{a}$.
点评 本题是一道求物质的质量分数的综合应用题目,学生只要列出关系式进行计算就可迅速解题,考查学生分析和解决问题的能力,难度中等.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
6.下列有关平衡常数的说法正确的是( )
| A. | 相同条件下,电离平衡常数越小,表示弱电解质的电离能力越弱 | |
| B. | 相同条件下,化学平衡常数越大,表示该反应的反应速率越大 | |
| C. | 其它条件不变时,升高温度,化学平衡常数一定增大 | |
| D. | 多元弱酸各步电离平衡常数相互关系为K1<K2<K3 |
7.下列分离方法不正确的是( )
| A. | 用过滤法除去Na2SO4溶液中的泥沙 | B. | 用蒸馏法分离溶液中的KCl和KNO3 | ||
| C. | 用萃取法将碘水中的I2萃取出来 | D. | 用蒸发法从NaCl溶液中得到NaCl |
4.常温下,将pH=3的强酸溶液和PH=12的强碱溶液混合,当混合液的pH等于11时,强酸与强碱溶液的体积比是( )
| A. | 9:2 | B. | 1:9 | C. | 10:1 | D. | 9:1 |
11.下列溶液中,溶质的物质的量浓度不是1mol•L-1的是( )
| A. | 10 g NaOH固体溶解在水中配成250 mL溶液 | |
| B. | 将80 g SO3溶于水并配成1 L的溶液 | |
| C. | 将0.5 mol•L-1的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 | |
| D. | 标况下,将22.4 L氯化氢气体溶于水配成1 L溶液 |
8.关于石油的说法不正确的是( )
| A. | 石油主要含C、H两种元素 | |
| B. | 石油是主要由各种烷烃、环烷烃和芳香烃所组成的混合物 | |
| C. | 石油有固定的沸点,故可分馏 | |
| D. | 石油分馏得到的汽油是混合物 |
5.下列表示方法中不正确的是:( )
| A. | 1 mol 氧 | B. | 1 mol O | C. | 1 mol O2 | D. | 1 mol O2 |
14.下列涉及有机化合物的说法正确的是( )
| A. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| B. | 丙烯分子中最多有6个原子共平面 | |
| C. | 甲苯硝化制对硝基甲苯与苯甲酸和乙醇反应制苯甲酸乙酯的反应类型不同 | |
| D. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,除去乙酸乙酯中乙酸可用饱和碳酸钠溶液 |
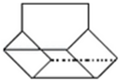 篮烷分子的键线式如图所示,试回答:
篮烷分子的键线式如图所示,试回答: