题目内容
下列有关离子方程式与所述事实相符合且正确的是( )
| A、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O | ||||
| B、Ba(OH)2溶液中逐滴滴加NaHSO4至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | ||||
C、用饱和氯化铁溶液和沸水反应制取氢氧化铁胶体:Fe3++3H2O
| ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2 Fe(OH)3=2 FeO42-+3Cl-+5H2O+4H+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.不能用盐酸酸化高锰酸钾溶液,否则高锰酸根离子能够氧化氯离子,干扰了双氧水的还原性的检验;
B.反应后的溶液为中性,则氢氧化钡与硫酸氢钠的物质的量之比为1:2,按照氢氧化钡的化学式组成书写离子方程式;
C.铁离子与沸水在加热条件下反应生成氢氧化铁胶体和氢离子;
D.碱性溶液中不会生成氢离子,反应产物错误.
B.反应后的溶液为中性,则氢氧化钡与硫酸氢钠的物质的量之比为1:2,按照氢氧化钡的化学式组成书写离子方程式;
C.铁离子与沸水在加热条件下反应生成氢氧化铁胶体和氢离子;
D.碱性溶液中不会生成氢离子,反应产物错误.
解答:
解:A.盐酸的氯离子能够被酸性高锰酸钾溶液氧化,干扰了实验结果,应该用硫酸酸化高锰酸钾溶液溶液,证明双氧水具有还原性的离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,故A错误;
B.Ba(OH)2溶液中逐滴滴加NaHSO4至中性,氢氧化钡与硫酸氢钠的物质的量之比为1:2,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故B错误;
C.用饱和氯化铁溶液和沸水反应制取氢氧化铁胶体,反应的离子方程式为:Fe3++3H2O
Fe(OH)3 (胶体)+3H+,故C正确;
D.强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,碱性溶液中反应产物不会生成氢离子,正确的离子方程式为:3ClO-+4OH-+2Fe(OH)3=2FeO42-+3Cl-+5H2O,故D错误;
故选C.
B.Ba(OH)2溶液中逐滴滴加NaHSO4至中性,氢氧化钡与硫酸氢钠的物质的量之比为1:2,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故B错误;
C.用饱和氯化铁溶液和沸水反应制取氢氧化铁胶体,反应的离子方程式为:Fe3++3H2O
| ||
D.强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,碱性溶液中反应产物不会生成氢离子,正确的离子方程式为:3ClO-+4OH-+2Fe(OH)3=2FeO42-+3Cl-+5H2O,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
短周期元素X和Y,X原子的电子层数为n,最外层电子数为(2n+1),Y原子最外层电子数是次外层电子数的3倍.下列说法一定正确的是( )
| A、X和Y都是非金属元素,其中X的最高化合价为+5价 |
| B、X与Y所能形成的化合物都是酸性氧化物 |
| C、元素X形成的盐化学式为KXO5 |
| D、X的氢化物极易溶于水,可以用来做喷泉实验 |
相等物质的量的CO和CO2相比较,下列有关叙述不正确的是( )
| A、它们所含的电子数目之比为1:1 |
| B、它们所含的O原子数目之比为1:2 |
| C、它们所含的C原子数目之比为1:1 |
| D、它们所含的原子总数目之比为2:3 |
下列反应:8NH3+3Cl2═6NH4Cl+N2,氧化剂和还原剂的质量比是( )
| A、8:3 |
| B、213:136 |
| C、34:213 |
| D、213:34 |
下列各组物质能在水溶液中大量共存的是( )
| A、Na+、K+、HCO3-、CO32- |
| B、Ca2+、Ba2+、HCO3-、OH- |
| C、Na+、HSO4-、S2-、SO32- |
| D、Ca2+、Na+、HCO3-、ClO- |
将PH=5的H2SO4溶液稀释500倍,稀释后,C(H+)与C(SO42-)的比值近似为( )
| A、1﹕1 | B、1﹕2 |
| C、10﹕1 | D、2﹕1 |
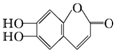 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是( )
| A、M的相对分子质量是180 |
| B、M与足量的NaOH溶液发生反应消耗2molNaOH |
| C、1mol M与足量NaHCO3反应生成2mol CO2 |
| D、1mol M最多能与3mol Br2发生反应 |