题目内容
(1)除去括号中的杂质,写出所加试剂的化学式与反应的离子方程式
①Fe2O3(Al2O3)所加试剂 离子方程式
②Na2SO4 (Na2CO3),所加试剂 ,离子方程式
③CO2(HCl)所加试剂 离子方程式 .
①Fe2O3(Al2O3)所加试剂
②Na2SO4 (Na2CO3),所加试剂
③CO2(HCl)所加试剂
考点:离子方程式的书写,物质的分离、提纯和除杂
专题:离子反应专题,化学实验基本操作
分析:①氧化铝为两性强氧化物,可以用氢氧化钠溶液除去氧化铁中的氧化铝;
②硫酸酸性强于碳酸,可以使用硫酸除去硫酸钠中的碳酸钠;
③氯化氢能够与饱和碳酸氢钠溶液反应,而二氧化碳不反应,可以用碳酸氢钠除去二氧化碳中的氯化氢.
②硫酸酸性强于碳酸,可以使用硫酸除去硫酸钠中的碳酸钠;
③氯化氢能够与饱和碳酸氢钠溶液反应,而二氧化碳不反应,可以用碳酸氢钠除去二氧化碳中的氯化氢.
解答:
解:①氧化铝是两性氧化物,能和氢氧化钠溶液反应,而氧化铁则不能与氢氧化钠反应,可以用氢氧化钠除去氧化铝,再过滤分离即可,
故答案为:NaOH溶液;Al2O3+2OH-═2AlO2-+H2O;
②硫酸能与碳酸根反应生成二氧化碳,反应离子方程式:CO32-+2H+=H2O+CO2↑,
故答案为:H2SO4;CO32-+2H+=H2O+CO2↑;
③氯化氢能与饱和NaHCO3溶液反应生成二氧化碳、水和氯化钠,二氧化碳和碳酸氢钠溶液不反应,可用饱和NaHCO3溶液除去二氧化碳中的氯化氢气体,反应的离子方程式为HCO3-+H+═CO2↑+H2O,
故答案为:饱和NaHCO3溶液;HCO3-+H+═CO2↑+H2O.
故答案为:NaOH溶液;Al2O3+2OH-═2AlO2-+H2O;
②硫酸能与碳酸根反应生成二氧化碳,反应离子方程式:CO32-+2H+=H2O+CO2↑,
故答案为:H2SO4;CO32-+2H+=H2O+CO2↑;
③氯化氢能与饱和NaHCO3溶液反应生成二氧化碳、水和氯化钠,二氧化碳和碳酸氢钠溶液不反应,可用饱和NaHCO3溶液除去二氧化碳中的氯化氢气体,反应的离子方程式为HCO3-+H+═CO2↑+H2O,
故答案为:饱和NaHCO3溶液;HCO3-+H+═CO2↑+H2O.
点评:本题考查物质的分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
下列各式中,属于水解方程式的是( )
| A、HCO3-+OH-=H2O+CO32- |
| B、NH3+H+=NH4+ |
| C、NH3?H2O?NH4++OH- |
| D、HCO3-+H2O?H2CO3+OH- |
下列说法正确的是( )
| A、9g水和标准状况下11.2LH2O所含分子数相同 |
| B、同温同压下,氦气的体积是氢气的两倍,则氦原子数与氢原子数之比为2:1 |
| C、同温同压,相同质量的CO和N2具有相同体积 |
| D、不同气体若体积不同,它们所含分子数也不同 |
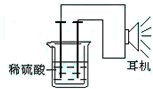 利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白:
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白: 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
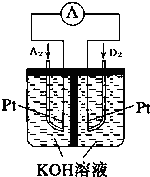
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
 A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答: