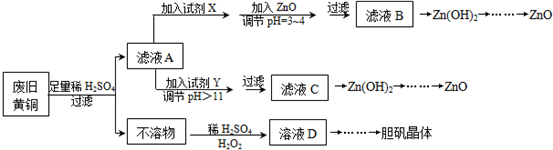
题目内容
在pH相等的①NH4Cl②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+ )大小顺序为 .
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:从两个角度考虑,一是相同pH的(NH4)2SO4与NH4Cl溶液的水解程度是否相等,二是NH4HSO4电离时产生H+使溶液呈酸性,NH4+的水解被抑制,以此来解答.
解答:
解:相同pH的(NH4)2SO4与NH4Cl溶液中,都是强酸弱碱盐,根据溶液呈电中性可判断二者NH4+浓度相等,由于NH4HSO4电离时产生H+使溶液呈酸性,NH4+的水解被抑制,因此NH4HSO4中NH4+的浓度小于(NH4)2SO4,
故答案应为:①=②>③.
故答案应为:①=②>③.
点评:本题考查离子浓度大小的比较,为高频考点,把握等pH时铵根离子浓度关系为解答的关键,侧重分析与应用能力的考查,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某种溶质的溶液的pH=2,向该溶液中加水到体积变为原来溶液体积的10倍,所得溶液的pH在2-3之间,则溶液中的溶质可能是 ①强酸 ②弱酸 ③强酸弱碱盐 ④强碱弱酸盐( )
| A、②④ | B、②③ | C、③④ | D、①② |
已知:甲+H2O→乙+丙,根据以上反应式进行的下列推断不合理的是( )
| A、甲为Fe丙为 Fe2O3 |
| B、甲为F2丙为O2 |
| C、甲为KH丙为 H2 |
| D、甲为CaC2丙为C2H2 |
反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每1mol CuSO4能氧化P的物质的量为( )
| A、0.2 mol |
| B、0.4 mol |
| C、0.6mol |
| D、2.2 mol |
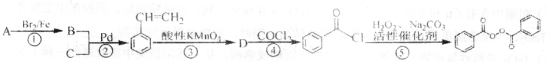
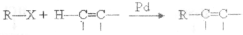
 ),在一定条件下能发生银镜反应,且1molE最多可得到4molAg;
),在一定条件下能发生银镜反应,且1molE最多可得到4molAg;