题目内容
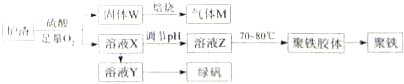
实验室可利用硫酸厂炉渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4?7H2O),聚铁的化学式为[Fe2(OH)n(SO4)3-0.5n]m,制备过程如图所示:下列说法不正确的是( )

| A、炉渣中FeS与硫酸和氧气的反应式为:4FeS+3O2+12H+═4Fe3++4S↓+6H2O |
| B、气体M的成分是SO2,通入双氧水得到硫酸,可循环使用 |
| C、溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数偏大 |
| D、向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸发浓缩、冷却结晶、过滤等步骤得到绿矾 |
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:分析流程可知炉渣加入硫酸溶液同时通入氧气得到固体W为氧化还原反应生成的硫单质和SiO2等,溶液X为含有Fe3+离子的溶液,调节溶液PH得到溶液Z加热得到聚铁,溶液X中加入铁反应生成硫酸亚铁溶液Y,蒸发结晶得到硫酸亚铁晶体
A、炉渣中FeS与硫酸和氧气反应生成硫单质硫酸铁和水;
B、固体W灼烧得到气体为二氧化硫;
C、若溶液Z的PH偏小,则聚铁中生成的氢氧根的含量减少,使铁的含量减少;
D、溶液X中加入过量铁粉,铁和硫酸铁溶液反应生成硫酸亚铁,通过蒸发浓缩,冷却结晶,过滤析出得到绿矾;
A、炉渣中FeS与硫酸和氧气反应生成硫单质硫酸铁和水;
B、固体W灼烧得到气体为二氧化硫;
C、若溶液Z的PH偏小,则聚铁中生成的氢氧根的含量减少,使铁的含量减少;
D、溶液X中加入过量铁粉,铁和硫酸铁溶液反应生成硫酸亚铁,通过蒸发浓缩,冷却结晶,过滤析出得到绿矾;
解答:
解:分析流程可知炉渣加入硫酸溶液同时通入氧气得到固体W为氧化还原反应生成的硫单质和SiO2等,溶液X为含有Fe3+离子的溶液,调节溶液PH得到溶液Z加热得到聚铁,溶液X中加入铁反应生成硫酸亚铁溶液Y,蒸发结晶得到硫酸亚铁晶体
A、炉渣中FeS与硫酸和氧气反应生成硫单质硫酸铁和水,反应的离子方程式为4FeS+3O2+12H+═4Fe3++4S↓+6H2O,故A正确;
B、炉渣加入硫酸溶液同时通入氧气得到固体W为氧化还原反应生成的硫单质和SiO2等,固体W灼烧得到气体为二氧化硫,故B正确;
C、用pH试纸测定方法为:将试纸放在表面皿上,用洁净的玻璃棒蘸取待测液,点在试纸的中央,然后与标准比色卡对比.氢氧化铁的含量比硫酸亚铁高,若溶液Z的PH偏小,则聚铁中生成的氢氧根的含量减少,使铁的含量减少,故C错误;
D、溶液X中加入过量铁粉,铁和硫酸铁溶液反应生成硫酸亚铁,通过蒸发浓缩,冷却结晶,过滤析出得到绿矾,符合晶体析出步骤,故D正确;
故选C.
A、炉渣中FeS与硫酸和氧气反应生成硫单质硫酸铁和水,反应的离子方程式为4FeS+3O2+12H+═4Fe3++4S↓+6H2O,故A正确;
B、炉渣加入硫酸溶液同时通入氧气得到固体W为氧化还原反应生成的硫单质和SiO2等,固体W灼烧得到气体为二氧化硫,故B正确;
C、用pH试纸测定方法为:将试纸放在表面皿上,用洁净的玻璃棒蘸取待测液,点在试纸的中央,然后与标准比色卡对比.氢氧化铁的含量比硫酸亚铁高,若溶液Z的PH偏小,则聚铁中生成的氢氧根的含量减少,使铁的含量减少,故C错误;
D、溶液X中加入过量铁粉,铁和硫酸铁溶液反应生成硫酸亚铁,通过蒸发浓缩,冷却结晶,过滤析出得到绿矾,符合晶体析出步骤,故D正确;
故选C.
点评:本题考查了物质分离和提纯的流程分析和方法判断,注意试剂选择和反应过程分析,掌握物质性质和实验过程是关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述中能肯定说明金属A比金属B的活泼的是( )
| A、A原子最外层电子数比B原子的最外层电子数少 |
| B、A原子电子层数比B原子的电子层数多 |
| C、1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 |
| D、常温时,A能从酸中置换出氢,而B不能 |
下列物质中不属于混合物的是( )
| A、白酒 | B、食醋 | C、生铁 | D、冰和水 |
你认为减少酸雨的产生可采取的措施是( )
①用煤作燃料 ②把工厂烟囱造高 ③化石燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源.
①用煤作燃料 ②把工厂烟囱造高 ③化石燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源.
| A、①②③ | B、②③④⑤ |
| C、③⑤ | D、①③④⑤ |
向25mL0.1mol/L NaOH溶液中逐滴滴加0.2moL/L CH3COOH溶液过程中溶液pH的变化曲线,当滴定至C点时,溶液中下列关系式错误的是( )


| A、c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B、c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C、c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| D、c(CH3COO-)-c(Na+)=c(H+)-c(OH-) |
关于如图所示的原电池,下列说法正在的是( )


| A、Zn为负极发生还原反应 |
| B、该装置能将电能转化为化学能 |
| C、电子由铜片通过导线流向锌片 |
| D、正极反应式为2H++2e═H2↑ |