题目内容
实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案:已知:NH4HCO3
NH3↑+H2O+CO2↑
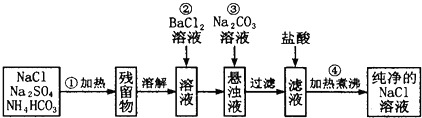
如果此方案正确,那么:
(1)操作②是否可改为加硝酸钡溶液? 理由是 .
(2)进行操作②后,如何判断SO42-已除尽,方法是
(3)操作③的目的是
(4)操作④的目的是 .
| ||

如果此方案正确,那么:
(1)操作②是否可改为加硝酸钡溶液?
(2)进行操作②后,如何判断SO42-已除尽,方法是
(3)操作③的目的是
(4)操作④的目的是
考点:粗盐提纯
专题:实验题
分析:(1)除杂的原则:除去杂质,不能引人新的杂质;
(2)钡离子能够与硫酸根离子产生硫酸钡沉淀,据此解答;
(3)要得到纯净的氯化钠,应除去加入氯化钡试剂引人的钡离子,碳酸钠能够与钡离子反应生成碳酸钡沉淀;
(4)要得到纯净的氯化钠,应除去反应生成的氯化氢,氯化氢在加热煮沸的情况下可以挥发出来.
(2)钡离子能够与硫酸根离子产生硫酸钡沉淀,据此解答;
(3)要得到纯净的氯化钠,应除去加入氯化钡试剂引人的钡离子,碳酸钠能够与钡离子反应生成碳酸钡沉淀;
(4)要得到纯净的氯化钠,应除去反应生成的氯化氢,氯化氢在加热煮沸的情况下可以挥发出来.
解答:
解:(1)加入硝酸钡溶液,硝酸钡和硫酸钠反应生成硫酸钡和硝酸钠,除去了硫酸根离子,但引入了硝酸根新的杂质离子,
故答案为:不可以;引入硝酸根杂质离子;
(2)加入过量氯化钡溶液,如果硫酸根离子为完全除去,则仍然含有硫酸根离子,能够与钡离子反应生成沉淀,所以检验硫酸根离子已除尽,可静止片刻在上层清液处,滴加一滴氯化钡溶液,不出现浑浊就说明硫酸根离子已经除尽;
故答案为:取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42-已除尽,反之则有;
(3)要得到纯净的氯化钠,应除去加入氯化钡试剂引人的钡离子,操作③加入碳酸钠溶液,碳酸钠与过量的氯化钠反应生成碳酸钡和氯化钠,除去过量的氯化钡,再过滤;先过滤而后加碳酸钠溶液,在加入碳酸钠溶液后生成的碳酸钡还需要过滤;
故答案为:除去过量的Ba2+;
(4)操作④加热煮沸溶液的目的是除去滤液中多余的氯化氢;
故答案为:除去滤液中多余的氯化氢.
故答案为:不可以;引入硝酸根杂质离子;
(2)加入过量氯化钡溶液,如果硫酸根离子为完全除去,则仍然含有硫酸根离子,能够与钡离子反应生成沉淀,所以检验硫酸根离子已除尽,可静止片刻在上层清液处,滴加一滴氯化钡溶液,不出现浑浊就说明硫酸根离子已经除尽;
故答案为:取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42-已除尽,反之则有;
(3)要得到纯净的氯化钠,应除去加入氯化钡试剂引人的钡离子,操作③加入碳酸钠溶液,碳酸钠与过量的氯化钠反应生成碳酸钡和氯化钠,除去过量的氯化钡,再过滤;先过滤而后加碳酸钠溶液,在加入碳酸钠溶液后生成的碳酸钡还需要过滤;
故答案为:除去过量的Ba2+;
(4)操作④加热煮沸溶液的目的是除去滤液中多余的氯化氢;
故答案为:除去滤液中多余的氯化氢.
点评:本题考查了氯化钠的分离与提纯,是高考频考点,明确杂质离子的性质和除杂的原则是解题关键,题目难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
25℃时,0.01mol?L-1 的H2SO4溶液中,由水电离出的c(H+)是( )
| A、0.01 mol?L-1 |
| B、0.02 mol?L-1 |
| C、1×10-12 mol?L-1 |
| D、5×10-13 mol?L-1 |