题目内容
10.下列叙述正确的是( )| A. | 浓硝酸、浓硫酸均能将木炭氧化成二氧化碳 | |
| B. | Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱 | |
| C. | Li、C、S分别在足量氧气中燃烧均生成一种相应氧化物 | |
| D. | NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
分析 A、浓硝酸、浓硫酸都具有强的氧化性,能够氧化碳;
B、Na2O2与水反应生成氢氧化钠,红热的Fe与水蒸气反应生成四氧化三铁;
C、Li、C、P分别在足量氧气中燃烧分别得到氧化锂、二氧化碳、五氧化二磷;
D、Na2CO3受热不分解.
解答 解:A、浓硝酸、浓硫酸都具有强的氧化性,能够氧化碳生成二氧化碳,故A正确;
B、Na2O2与水反应生成氢氧化钠,红热的Fe与水蒸气反应生成四氧化三铁,不生成碱,故B错误;
C、Li、C、P分别在足量氧气中燃烧分别得到氧化锂、二氧化碳、五氧化二磷,均生成一种相应氧化物,故C正确;
D、Na2CO3受热不分解,无气体生成,故D错误;
故选AC.
点评 本题考查了物质性质的分析判断,注意物质特殊性质的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
20.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 2.4g金属镁变为镁离子时所含电子数为NA | |
| B. | 1mol•L-1的A1Cl3溶液中,Cl-离子的数目为3NA | |
| C. | 标准状况下,22.4LSO3含有的分子数为NA | |
| D. | 常温常压下,16g O2和O3的混合气体所含分子数为NA |
1.下列说法不正确的是( )
| A. | 按系统命名法,化合物 的名称为2-甲基-3,4-二乙基己烷 的名称为2-甲基-3,4-二乙基己烷 | |
| B. | 等质量的甲烷、乙醇、乙醛分别充分燃烧,所耗用氧气的量依次减小 | |
| C. | 下列物质的沸点按由低到高顺序为:(CH3)2CHCH3<(CH3)4C<(CH3)2CHCH2CH3<CH3(CH2)3CH3 | |
| D. |  与 与 互为同系物 互为同系物 |
18.下列物质均有漂白作用,其漂白原理相同的是( )
①过氧化钠 ②次氯酸 ③双氧水 ④活性炭 ⑤二氧化硫 ⑥臭氧.
①过氧化钠 ②次氯酸 ③双氧水 ④活性炭 ⑤二氧化硫 ⑥臭氧.
| A. | ①②③⑤ | B. | 只有①②③⑥ | C. | ②③④⑤ | D. | 只有①③⑤⑥ |
5.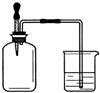 如右图所示,集气瓶 内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )
如右图所示,集气瓶 内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )
①CO、O2 ②Cl2、NH3 ③NO2、O2 ④N2、H2.
 如右图所示,集气瓶 内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )
如右图所示,集气瓶 内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )①CO、O2 ②Cl2、NH3 ③NO2、O2 ④N2、H2.
| A. | ①② | B. | ②④ | C. | ②③ | D. | ③④ |
15.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H1=-Q1 KJ/mol
2H2(g)+O2(g)═2H2O(g)△H2=-Q2 KJ/mol
2H2(g)+O2(g)═2H2O(1)△H3=-Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
2H2(g)+O2(g)═2H2O(g)△H2=-Q2 KJ/mol
2H2(g)+O2(g)═2H2O(1)△H3=-Q3KJ/mol
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则下列说法正确的是( )
| A. | 放出的热量为(0.4Q1+0.05Q3)KJ | B. | 放出的热量为(0.4Q1+0.05Q2)KJ | ||
| C. | △H2=△H3 | D. | △H2<△H3 |
2.生物学家研究发现白蚁信息素有: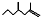 (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),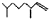 (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)3CH=CH-CH=CH(CH2)3CH3.下列说法正确的是( )
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)3CH=CH-CH=CH(CH2)3CH3.下列说法正确的是( )
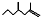 (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),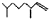 (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)3CH=CH-CH=CH(CH2)3CH3.下列说法正确的是( )
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)3CH=CH-CH=CH(CH2)3CH3.下列说法正确的是( )| A. | 以上三种信息素互为同系物 | |
| B. | 以上三种信息素均能使溴的四氯化碳溶液褪色 | |
| C. | 2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同分异构体 | |
| D. | 家蚕的性信息素与1molBr2加成产物只有一种 |
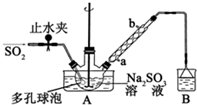 次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解,在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图:
次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解,在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图: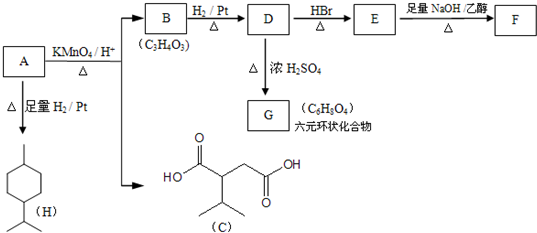
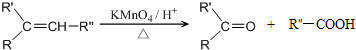
 .
. .
. .
.