题目内容
8.下列关于确定官能团的方法不正确的是( )| A. | 加入NaHCO3溶液产生气体,表示含有-COOH或酚羟基 | |
| B. | 遇浓硝酸变黄,则表明该物质是含有苯环结构的蛋白质 | |
| C. | 加入新制的Cu(OH)2悬浊液,加热煮沸有红色沉淀生成,或加入银氨溶液加热有银镜生成,表示含有-CHO | |
| D. | 某有机物与醋酸反应,相对分子质量增加42,则含有1个-OH;增加84,则含有2个-OH |
分析 A.酚羟基与碳酸氢钠溶液不反应;
B.含有苯环结构的蛋白质与硝酸发生颜色反应;
C.醛基可与氢氧化铜浊液或银氨溶液发生氧化还原反应;
D.根据R-OH~ROOCCH3的质量关系判断.
解答 解:A.酚类的酸性比碳酸弱,酚羟基与碳酸氢钠溶液不反应,故A错误;
B.含有苯环结构的蛋白质与硝酸发生颜色反应,变为黄色,故B正确;
C.醛基可与氢氧化铜浊液或银氨溶液发生氧化还原反应,故C正确;
D.由R-OH~ROOCCH3的质量关系可知,反应质量增大部分相当于“OCCH2”,式量为42,则有机物与醋酸反应,相对分子质量增加42,则含有1个-OH;增加84,则含有2个-OH,故D正确.
故选A.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物官能团的变化,把握有机反应的规律,难度不大.

练习册系列答案
相关题目
18.钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展.
(1)Al(NO3)3是制备钠硫电池部件的原料之一.由于Al(NO3)3容易吸收环境中的水分,需要对其进行定量分析.具体步骤如图所示:
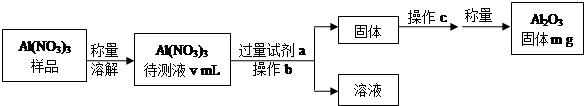
①加入试剂a后发生反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH4+.
②操作b为过滤,操作c为洗涤、灼烧(或加热)、冷却.
③Al(NO3)3待测液中,c (Al3+)=$\frac{1000m}{51v}$mol•L-1(用m、v表示).
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
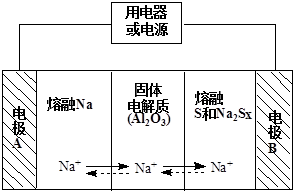
①根据下表数据,请你判断该电池工作的适宜温度应控制在c范围内(填字母序号).
a.100℃以下 b.100℃~300℃c.300℃~350℃d.350℃~2050℃
②放电时,电极A为负极.
③放电时,内电路中Na+的移动方向为从A到B(填“从A到B”或“从B到A”).
④充电时,总反应为Na2Sx═2Na+xS(3<x<5),则阳极的电极反应式为Sx2--2e-═xS.
(1)Al(NO3)3是制备钠硫电池部件的原料之一.由于Al(NO3)3容易吸收环境中的水分,需要对其进行定量分析.具体步骤如图所示:

①加入试剂a后发生反应的离子方程式为Al3++3NH3•H2O═Al(OH)3↓+3NH4+.
②操作b为过滤,操作c为洗涤、灼烧(或加热)、冷却.
③Al(NO3)3待测液中,c (Al3+)=$\frac{1000m}{51v}$mol•L-1(用m、v表示).
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:

①根据下表数据,请你判断该电池工作的适宜温度应控制在c范围内(填字母序号).
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
②放电时,电极A为负极.
③放电时,内电路中Na+的移动方向为从A到B(填“从A到B”或“从B到A”).
④充电时,总反应为Na2Sx═2Na+xS(3<x<5),则阳极的电极反应式为Sx2--2e-═xS.
19.下列分子只表示一种物质的是( )
| A. | C3H7Cl | B. | C3H8 | C. | C3H6 | D. | C |
16.下列说法正确的是( )
| A. | 原子最外层电子数等于或大于3的元素一定是主族元素 | |
| B. | 原子最外层只有1个电子的元素一定是第IA族元素 | |
| C. | 最外层电子数比次外层电子数多的元素一定位于第二周期 | |
| D. | 某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期 |
3.下列关于卤代烃的说法正确的是( )
| A. | 在卤代烃中,卤素原子与碳原子间形成共价键 | |
| B. | 在溴乙烷(CH3CH2Br)分子中,溴元素的存在形式为溴离子 | |
| C. | 聚四氟乙烯(塑料王)为高分子化合物,不属于卤代烃 | |
| D. | 卤代烃的沸点比相应烷烃的沸点低 |

 二氧化硫和氮的氧化物是大气的主要污染物,防止和治理环境污染是当前环保工作的重要研究内容之一.
二氧化硫和氮的氧化物是大气的主要污染物,防止和治理环境污染是当前环保工作的重要研究内容之一.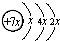 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题: .
.